Serviços Personalizados
Artigo
Links relacionados
Compartilhar
Odontologia Clínico-Científica (Online)
versão On-line ISSN 1677-3888
Odontol. Clín.-Cient. (Online) vol.10 no.2 Recife Abr./Jun. 2011
ARTIGO DE REVISÃO / REVIEW ARTICLE
Cárie e erosão dentária: uma breve revisão
Dental caries and erosion: a soon review
Dayane Franco Barros MangueiraI; Isabela Albuquerque PassosI; Ana Maria Barros Chaves PereiraII; Andressa Feitosa Bezerra de OliveiraII
I Profa. Ms. do Departamento de Odontologia Restauradora da Universidade Federal da Paraíba-UFPB
II Profa. Dra. do Departamento de Morfologia da Universidade Federal da Paraíba-UFPB
RESUMO
O esmalte dentário é um tecido duro, submetido constantemente aos processos de des e remineralização pelo contato com os fluidos bucais. Acredita-se que é necessário compreender o mecanismo de formação do esmalte para entender como os ácidos orgânicos e inorgânicos interferem na sua estrutura por visão microscópica e clínica. Desta forma, o objetivo desse trabalho foi realizar uma revisão da literatura sobre os aspectos clínicos e histopatológicos de dois tipos de desgaste dentário: cárie e erosão. Enfatiza-se que apesar da cárie e da erosão serem resultado de processos de perda de tecido do dente, o mecanismo de ação do agente etiológico é diferenciado a nível microestrutural, repercutindo em aspectos clínicos distintos.
Descritores: Erosão Dentária, Cárie Dentária, Desgaste dos dentes.
ABSTRACT
Dental enamel is a hard tissue, des and remineralization processes is frequently because buccal fluids constant expouse. It is believed that is necessary to understand the enamel formation mechanism to understand as the organic and inorganic acids interfere in structure one for microscopic and clinical vision. This way, the aim of this work was carry out literature review about clinical and histopatological aspects of two types of dental wear: caries and erosion. It is emphasized that dental caries and erosion resulted of loss tooth tissue processes, the etiological agent action mechanism is diff erentiated by microstrutural and clinical level.
Keywords: Tooth Erosion, Dental Caries, Tooth Wear.
INTRODUÇÃO
O esmalte normal e hígido é constituído de cristais de hidroxiapatita firmemente reunidos, que lhe dão uma aparência semelhante ao vidro, sendo, portanto, translúcido1. Esses cristais do esmalte estão organizados em prismas e no esmalte interprismático. Cada cristal está separado de seus vizinhos por minúsculos espaços intercristalinos que são preenchidos por água e material orgânico2.
A cárie dentária é uma doença crônica que progride de forma lenta3. Seu primeiro sinal clínico é representado pela mancha branca ativa podendo ser reversível diante da aplicação de flúor, principalmente na forma de verniz4. Na ausência do tratamento, a lesão evolui até a destruição da estrutura dentária. Os sinais da doença podem variar desde perdas minerais em nível ultra-estrutural até a destruição total do elemento1. O diagnóstico de cárie dentária envolve conhecimento da interação entre os diversos fatores causais5.
A partir do diagnóstico de cárie dentária recomendado pela OMS, estudos de prevalência têm se desenvolvido como nos estudos de Moreira, Rosenblatt e Passos6 (2007) na cidade de João Pessoa, em que os achados evidenciaram prevalência da doença de 51,6% em escolas públicas e 9,3% em escolas particulares na faixa etária de 12 a 15 anos. Já no SB Brasil 2003 observou-se que na região Nordeste, a média de CPOD foi de 3,19 aos 12 anos, enquanto na faixa etária de 15 a 19 anos, foi de 6,34. Em nível nacional, o CPOD aos 12 anos e de 15 a 19 anos foi de 2,78 e 6,17, respectivamente7.
Com o declínio da cárie dentária8, outros agravos à saúde bucal têm suscitado maior atenção da comunidade científica, dentre eles erosão dentária. Assim como a cárie dentária, esse processo pode ocorrer em indivíduos nas mais diversas idades, envolvendo tanto a dentição decídua como a dentição permanente9.
A erosão dentária é um tipo de desgaste que ocorre na estrutura do dente caracterizada pela perda progressiva de tecido, causada pela ação de substâncias químicas sobre a superfície exposta na cavidade bucal, não envolvendo bactérias10. As substâncias químicas que provocam erosão dentária podem ser provenientes de fontes extrínsecas, como a dieta, e intrínsecas, a exemplo do ácido gástrico11.
O diagnóstico diferencial da erosão dentária envolve conhecimento de lesões cervicais como abrasão: clinicamente caracterizada por uma lesão semelhante a uma cunha de superfície de aspecto polido; atrição: clinicamente, uma superfície com a aparência extremamente polida e lisa, além da formação de múltiplas facetas e abfração: clinicamente, os dentes se apresentam em forma de lâmina e a lesão tem um aspecto de cunha, limitada à área cervical do dente e com término cavitário nítido12.
Dados de prevalência indicam 19,9% para a erosão dentária na cidade de João Pessoa em escolares na faixa etária de 6 a 12 anos13. Já em Recife, a prevalência encontrada foi menor, 3.4%, na faixa etária de 5 a 12 anos14.
Devido à necessidade de se realizar um diagnóstico precoce e preciso das lesões que acometem a cavidade oral, o presente trabalho teve como objetivo realizar uma revisão da literatura, abordando as características clínicas e histopatológicas da cárie e da erosão dentária.
DESENVOLVIMENTO
Amelogênese
É necessário compreender o mecanismo de formação do esmalte para entender como os ácidos orgânicos e inorgânicos interferem na sua estrutura.
Assim, o esmalte dentário é formado pelos ameloblastos originados da lâmina dentária do epitélio oral, que se diferenciam para secretarem a matriz extracelular. As fases da amelogênese podem ser divididas, didaticamente, em pré-secretora, secretora e de maturação. Na fase pré-secretora, os ameloblastos adquirem seu fenótipo, se diferenciam em células polarizadas e se preparam para secretar a matriz orgânica do esmalte. O estágio secretório é caracterizado pela deposição de proteínas como as amelogeninas, tuftelinas, ameloblastinas e metaloproteínas. Em seguida, a fase de maturação é marcada pelos ciclos de modulação em que os ameloblastos removem as proteínas e depositam minerais15. Após formar o esmalte, os ameloblastos perdem sua polaridade e formam o epitélio reduzido do esmalte que será rompido com a erupção dentária.
Nas fases iniciais da amelogênese o esmalte é constituído por 20 a 30% de matriz protéica. Ao final do processo, esse tecido apresenta os cristais de apatita organizados em prismas de maneira densa e imbricada, estendendo-se desde a junção amelodentinária até a superfície externa do dente16.
O esmalte é o tecido mais duro do corpo humano pela sua constituição ser de 97 % de componentes inorgânicos e apenas 3 % de matéria orgânica, sendo 2 % de proteínas não colágenas e 1% de água17.
Salienta-se que o nível mineral varia de acordo com a localização, o esmalte de um dente erupcionado é mais mineralizado na superfície externa pelo contato constante com a saliva rica em íons como cálcio e flúor18.
Aspectos clínicos da cárie x erosão dentária
O acúmulo de depósitos microbianos na superfície do esmalte é fator fundamental para o desenvolvimento do processo de cárie. Após permanecer 14 dias com biofilme completamente inalterado, as alterações do esmalte tornam-se macroscopicamente visíveis após secagem com ar, caracterizando- se como alterações esbranquiçadas e opacas, representando o primeiro sinal clínico da cárie dentária. Associado a isso, tem-se uma lesão subsuperficial formado pela desmineralização1.
Após 3 a 4 semanas com biofilme inalterado, as alterações clinicamente detectáveis podem ser imediatamente visualizadas, sem a secagem com ar. A perda mineral localizada sob a superfície externa torna-se mais extensa e em constante processo de aumento. A lesão de mancha branca apresenta uma característica superficial calcária que lembra o giz, tornando-o opaco, já que perde sua aparência brilhante1. A aparência clínica dessas lesões brancas ou manchas brancas é causada pela perda da subcamada de esmalte, resultando na perda da translucidez19.
Segundo Maltz e Carvalho20 (2003) manchas rugosas e opacas indicam lesões ativas, enquanto que manchas lisas e brilhantes indicam lesões inativas. Nas áreas comprometidas que não forem mantidas livres de biofilme, o processo continuará, e o esmalte será destruído progressivamente, com aumento gradual da cavidade.
A progressão das perdas minerais em relação ao tempo são perceptíveis inicialmente pela microscopia eletrônica, avançando à microscopia óptica, e se tornam visíveis no estágio de lesão no esmalte, evoluindo para formação da cavidade até a destruição total da estrutura dentária1.
Com relação à erosão dentária, destaca-se a diminuição do brilho no esmalte, caracterizando-se por uma lesão arredondada e pela ausência de mancha branca21.
Três estágios de destruição do tecido dentário podem ser destacados no processo de desenvolvimento da erosão dentária: (1) perda de substâncias orgânicas salivares, que cobrem a superfície dentária, seguido da (2) perda de mineral da superfície do dente devido à presença de um agente descalcificante e, por último, (3) a destruição da superfície dentária descalcificada por uma ação bioquímica e/ou biofísica e/ou mecânica10.
Clinicamente, a lesão de erosão é caracterizada por uma superfície lisa, em forma de "U" ou pires, mostrando uma lesão larga e rasa, com superfície polida, geralmente, na ausência de biofilme dentário. Posteriormente, pode ocorrer a perda do contorno original, resultando em uma lesão côncava, delimitada, com exposição de dentina e esmalte saliente ao redor da lesão22.
Quando esse tipo de lesão acomete elementos que possuem restaurações, de amálgama ou de resina composta, as mesmas permanecem intactas e se projetam acima das superfícies dentárias23.
Como consequência da erosão, pode haver exposição pulpar, hipersensibilidade dentinária, diastemas, bordas incisais finas ou fraturadas, perda de dimensão vertical, pseudo mordida aberta e comprometimento estético24.
Aspectos histopatológicos da cárie x erosão dentária
Em virtude do seu elevado conteúdo mineral, o esmalte dentário pode ser observado na Microscopia Óptica, por meio das técnicas histológicas de desgaste e desmineralização. A técnica de desgaste não preserva as células do tecido, mas permite um estudo minucioso da matriz inorgânica. Enquanto a técnica de desmineralização permite o estudo minucioso das células e da matéria orgânica do tecido após a retirada de seus componentes inorgânicos25.
O caráter incremental da síntese do esmalte origina as estrias de Retzius, evidenciadas na superfície adamantina pelas perenquimáceas16. Pelo fato das Estrias de Retzius serem espaço dispostos em toda extensão do esmalte17, acredita-se que elas possam facilitar a difusão dos ácidos durante o processo de formação da cárie e da erosão, juntamente com as lamelas do esmalte.
Na erosão dentária, a superfície adamantina apresenta áreas de aspecto morfológico diferente do esmalte normal, devido o desgaste da superfície, quando observado em Microscópico Eletrônico de Varredura (MEV). A superfície dentária exposta a ácidos de pH < 4,5 resulta na destruição do esmalte em camadas26 (Figura 1) explicando o fato de alguns autores afirmarem que na erosão nenhuma remineralização pode ser esperada, já que para ocorrer esse processo é necessário a presença dos cristais desmineralizados27. Adicionado a isso, o esmalte completamente formado é um tecido acelular e sem capacidade de renovação28.
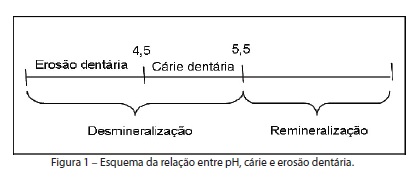
Enquanto na cárie dentária, a exposição aos ácidos orgânicos desencadeia a formação de uma lesão subsuperficial por perda de 50% de mineral, mas a camada externa do esmalte é mantida intacta, o que permite sua remineralização29.
A solubilidade da apatita do esmalte em um pH próximo a 3 é aproximadamente 100 vezes maior que em um pH 5, no qual a lesão de cárie se desenvolve27. A solubilidade parece estar diretamente relacionada ao tipo de dente envolvido, sendo a progressão da erosão mais rápida no esmalte bovino, seguido do decíduo e do permanente. Além disso, o fator temperatura e tempo de exposição dos ácidos a superfície adamantina atuam diretamente no desenvolvimento da erosão30.
Um fator protetor a superfície do esmalte é a saliva que forma a película adquirida do esmalte, a qual reduz o efeito desmineralizador dos produtos ácidos por dificultar a difusão do ácido para superfície adamantina2,26.
CONSIDERAÇÕES FINAIS
A partir da literatura pesquisada, considera-se de fundamental importância para o cirurgião-dentista o conhecimento sobre o processo de formação e características clínicas e histopatológicas próprias dos dois tipos de desgaste abordados.
Essa revisão da literatura contribuiu no sentido de complementar e precisar o diagnóstico da cárie e erosão dentária, para que as orientações e o tratamento adequados sejam logo realizados.
Estudos adicionais devem ser realizados sob o ponto de vista histopatológico da erosão dentária, visto que a literatura ainda é escassa nesse sentido.
REFERÊNCIAS
1. Fejerskov O, Kidd EAM. Cárie dentária: a doença e seu tratamento clínico. São Paulo: Santos; 2005. [ Links ]
2. Hannig M, Balz M. Influence of in vivo formed salivary pellicle on enamel erosion. Caries Res 1999; 33:372-9.
3. Grewal H, Verma M, Kumar A. Prevalence and dental caries and treatment needs in the rural child population of Nainital district, Uttaranchal, J Indian Soc Pedod Prevent Dent 2009; 27(4): 224-6.
4. Ferreira JMS et al. Therapeutic effect of two fluoride varnishes on white spot lesions: a randomized clinical trial. Braz Oral Res [online]. 2009; 23(4):446-51.
5. Carounanidy U, Sathyanarayanan R. Dental caries: a complete changeover (Part II)-Changeover in the diagnosis and prognosis. J Conserv Dent. 2009;12(3):87-100.
6. Moreira PVL, Rosenblatt A, Passos IA. Prevalência de cárie em adolescentes de escolas públicas e privadas na cidade de João Pessoa, Paraíba, Brasil. Ciênc. saúde coletiva. 2007;12(5):1229-36.
7. Brasil. Ministério da Saúde. Projeto SB Brasil 2003 Condições de saúde bucal da população brasileira 2002-2003. Resultados principais. 2003. [acessado 2010 jul 05]: [cerca de 52 p.] Disponível em: bvsms.saude.gov.br/bvs/publicacoes/projeto_sb2004.pdf
8. Gushi LL et al. Cárie dentária e necessidades de tratamento em adolescentes do estado de São Paulo, 1998 e 2002. Rev Saúde Pública. 2008;42(3):480-6.
9. Peres KG; Armênio MF. Erosão dental. In: Antunes JLF; Peres MA. Fundamentos da odontologia epidemiologia da saúde bucal. Guanabara Koogan: Rio de Janeiro, 2006.
10. Zero DT. Etiology of dental erosion- extrinsic factors. Eur J Oral Sci 1996;104:162-77.
11. Imfeld T. Dental erosion. Definition, classification and links. Eur J Oral Sci. 1996; 104(2):151-5.
12. Mangueira DFB, Passos IA, Oliveira AFB, Sampaio FC. Erosão dentária: etiologia, diagnóstico, prevalência e medidas preventivas Arquivos em Odontologia 2009; 45 (4): 220-5.
13. Mangueira DF, Sampaio FC, Oliveira AF. Association between socioeconomic factors and dental erosion in Brazilian schoolchildren. J Public Health Dent 2009;69(4):254-9.
14. Araújo NC, Massoni ACLT, Katz CRT, Rosenblatt A. Dental erosion and consumption of industrialized beverages in a group of children in Recife/Pernambuco, Brazil. Rev. odonto ciênc 2009;24(2):120-3.
15. Jälevik B, Dietz W, Noren JG. Scanning electron micrograph analysis of hypomineralized enamel in permanent first molars. Int J Paediatr Dent. 2005; 15(4):233-40.
16. Smith TM. Experimental determination of the periodicity of incremental features in enamel. J. Anat 2006; 208:99-113.
17. Katchburian E, Arana V. Histologia e embriologia oral. 1ª.ed. Rio de Janeiro: Guanabara Koogan; 1996.
18. Amaechi BT, Higham SM. Eroded enamel lesion remineralization by saliva as a possible factor in the site-specificity of human dental erosion. Archs oral Biol. 2001; 46:697-703.
19. Zero DT. Dental caries process. Dent Clin North Amer. 1999;43(4):635-63.
20. Maltz M, Carvalho J. Diagnóstico da doença cárie. In: Kriger L. Promoção de saúde bucal. 3 ed. São Paulo: Artes Médicas; 2003.
21. Sobral MAP, Garone Netto N. Aspectos clínicos da etiologia da hipersensibilidade dentinária cervical. Rev Odontol Univ São Paulo. 1999; 13(2): 189-95.
22. Benevius J, L'Estrange P, Angmar- M°ansson B. Erosion: guidelines for the general practitioner. Austr Dent J 1988; 33(5): 407-11.
23. Baratieri LN et al. Odontologia restauradora: fundamentos e possibilidades. São Paulo: Santos; 2001.
24. Pegoraro CN et al. Perimólise: etiologia, diagnóstico e prevenção. Revista da APCD. 2000; 156-61.
25. Junqueira LC, Carneiro J. Tecido ósseo. In: Histologia básica. 9 ed. Guanabara Koogan: Rio de Janeiro; 1999.
26. Nekrashevych Y, Stösser L. Protective influence of experimentally formed salivary pellicle on enamel erosion. Caries Res. 2003; 37:225-31.
27. ten Cate JM, Larsen MJ, Pearce EIF, Fejerskov O. Interações químicas entre o dente e os fluidos orais. In: Fejerskov O, Kidd E. Cárie dentária. A doença e o seu tratamento. Ed Santos: São Paulo; P. 50-69. 2005.
28. Robinson C. A developing enamel matrix: nature and function. Eur J Oral Sci. 1998; 106:282-91.
29. Moreno EC. Role of Ca-P-F in caries prevention. Chemical aspects. Int Dent J. 1993; 43:71-80.
30. Amaechi BT, Highman SM, Edgar WM. Factors influencing the development of dental erosion in vitro: enamel type, temperature and exposure time. J. Rehab. 1999; 26:624-30.
 Endereço para correspondência:
Endereço para correspondência:
Dayane Franco Barros Mangueira
R. Helena Meira Lima, 75, Tambaú
João Pessoa-PB CEP:58039-080
E-mail: dayanemangueira@gmail.com
Recebido para publicação: 19/02/10
Encaminhado para reformulação: 16/06/10
Aceito para publicação: 05/08/10