Serviços Personalizados
Artigo
Links relacionados
Compartilhar
Revista Brasileira de Odontologia
versão On-line ISSN 1984-3747versão impressa ISSN 0034-7272
Rev. Bras. Odontol. vol.70 no.1 Rio de Janeiro Jan./Jun. 2013
ARTIGO ORIGINAL / ORIGINAL ARTICLE
Caracterização das superfícies de implantes dentais comerciais em MEV/EDS
Characterization of the surfaces of dental implants commercial in MEV/EDS
João Galan Jr.I;Ronan Miranda VieiraII
I Professor Titular de Materiais Dentários da Uerj
II Mestre em Reabilitação Oral pela UVA
RESUMO
O objetivo foi caracterizar morfológica e quimicamente os diferentes sistemas de implantes. As amostras avaliadas apresentaram características de rugosidade superficial exceto para os implantes Externo Laser®, tendo os implantes Titamax® e Implant External Hex® apresentado características de rugosidade promovidas por jateamento de partículas, e o Osseotite®, Implant Revolution® e Máster Porous® apresentaram características porosas. Pode-se concluir que na análise das amostras houve um aumento de impurezas após modificações na superfície. Os elementos encontrados sugerem que os implantes apresentam deficiências considerando o processo de limpeza final antes da comercialização.
Palavras-chave: MEV; EDS; implantes dentais; superfície química; morfologia superficial.
ABSTRACT
The purpose was to characterize the surfaces morphology and the superficial chemical composition of related osseointegrable implant systems. The evaluated samples presented characteristics of superficial roughness except for Externo Laser® implants, having Titamax® and Implant External Hex® implants presented roughness characteristics promoted by blasting of particles and the Osseotite®, Implant Revolution® and Máster Porous® implants presented porous characteristics.There are morphologic differences among implants of different companies.
Keywords: MEV; EDS; dental implants; chemistry surface; morphology surface.
Introdução
Com o advento da osseointegração, implantes dentais começaram a ser utilizados de forma disseminada, com o objetivo principal de minimizar as consequências do edentulismo, seja ele total ou parcial. Em decorrência disso, muitas técnicas e propostas para a realização da Implantodontia foram preconizadas, porém, muitas delas eram baseadas apenas em experiências anteriores, que resultava em um alto índice de insucesso. Isto fez com que pesquisadores propusessem e descrevessem que o sucesso de um implante está na dependência da interrelação de vários componentes, dentre os quais se incluem as características próprias da superfície do implante e a contaminação do mesmo por micro-organismos que expressam fatores de virulência capazes de lesar os tecidos peri-implantares1.
Nos tecidos vivos, o implante dentário é considerado um corpo estranho, o qual interage de várias maneiras com o ambiente. Isso pode insultar a vida química, fisiológica ou mecânica 2.
Metais de implante têm sido selecionados baseando-se em alguns fatores: suas propriedades biomecânicas, experiência prévia no processamento, tratamento, usinagem e acabamento, bem como para o acondicionamento para esterilização 3.
Quando exposto no ar, o titânio (Ti) forma imediatamente uma camada de óxido que alcança a espessura de 2 a 10 nm em um segundo e provê resistência à corrosão. Por causa desta grande passividade, controle de espessura, rápida formação, habilidade de reparo de si mesmo quando danificado, resistência ao ataque químico, atividade catalisadora para um número de reações químicas e, compatível módulo de elasticidade entre o óxido de titânio e o osso, o Ti é o material de escolha para implantes endósseos 3,4.
O titânio comercialmente puro (Ti cp) tem sido o material de escolha para a confecção dos implantes endósseos, pois é um metal que possibilita reação tecidual favorável, estabilidade química dos componentes, estimula a atividade celular na formação de matriz óssea, tem elevada resistência à corrosão e não provoca reações de hipersensibilidade ou imunológicas. A camada de dióxido de titânio (TiO2) é responsável pela adaptação íntima, denominada osseointegração ou anquilose funcional, entre o osso mineralizado e a superfície do implante 4,5,6,7,8,9,10. Vários são os tipos de fenômenos na superfície que influenciam a interação entre o titânio e os tecidos biológicos. As propriedades de superfície como a molhabilidade, carga, estabilidade microestrutural e química são alguns parâmetros que devem ser considerados para interações em que o contato com o sangue, moléculas de água e pequenos íons procuram primeiramente a superfície, seguida de proteínas de alto peso molecular e por células (plaquetas e leucócitos) determinando as interações com o material; as interações do sistema biológico ao redor serão com o material, a fase inorgânica, água e íons, absorção pequena e larga de biomoléculas ou a adesão inicial celular 3,6,10.
O efeito das superfícies rugosas na formação da camada de óxido e na agregação celular tem sido estudado. No entanto, não foram observadas alterações na camada do óxido e implicações biológicas. Além disso, a agregação celular parece ser mais favorável para rugosidades produzidas por jateamento (Ra = 0.7 a 0.9 μm) quando comparadas com as polidas (Ra = 0.04 μm) ou espécimes "arranhados"(Ra = 0.1 a 0.2 μm), sendo constituídos principalmente de TIO2, com oxigênio, carbono e nitrogênio como contaminantes. Contaminantes inorgânicos incluindo pequenas moléculas de sódio, cloro, sílica, cálcio, fósforo e enxofre são encontrados, mas não em todas as amostras. Amostras com espessura da camada de óxido menor que 100 nm são consideradas amorfas 8,11.
Enquanto é realizada a implantação, uma camada de óxido hidratado cresce sobre o titânio, o que já é previsto. A interação entre e osso e o metal depende da atividade metabólica no sitio da implantação. Modelos experimentais mostram que titânio in vitro forma um composto de peróxido de titânio previsto para interagir com o peróxido de hidrogênio, um tipo que se relaciona com células inflamatórias 6. Contudo, o significado biológico não é claro, mas, isto foi sugerido que in vivo a interação entre o titânio e o peróxido de hidrogênio poderia influenciar na dissolução do material nos tecidos e uma inicial resposta inflamatória, devido o fechamento do tecido sobre o implante 4. O titânio, por meio de sua superfície, participa da ativação do sistema complemento imunológico e também ativo intrinsecamente a coagulação sanguínea. Além disso, ele é fortemente trombogênico quando contatado. O osso aparece separado da superfície do implante por uma fina camada de 50 nm de espessura 5. Este é um achado consistente em pesquisas com animais. O osso pode crescer sobre a superfície do implante, sugerindo que a influência do desenho do implante, procedimentos cirúrgicos e carga mecânica são importantes 3,5. Esses efeitos são fortemente dependentes das propriedades superficiais dos materiais e das modificações destas propriedades pelo manuseio e pelos sistemas biológicos 3,5,7.
Diferentes tratamentos de superfície são usados para mudar a topografia e a rugosidade do titânio a fim de aumentar a osseointegração levando, geralmente, a uma melhor ancoragem mecânica e biológica. O condicionamento e o ataque ácido são largamente utilizados e podem ser usados na forma simples ou após um jateamento (processo conhecido como SLA) demonstrando um aumento nos níveis e quantidade de formação óssea sobre a superfície do implante 8,12.
Tendo em vista que o condicionamento ácido causa diferentes graus de corrosão nos implantes e modifica a sua superfície com o aumento de rugosidade superficial 3,12,13 descreveram uma técnica que abrange superfícies de titânio puro, dependendo da concentração do ácido e tempo de exposição. Desta forma, é possível obter-se, com o mesmo tratamento químico, tanto grandes depressões quanto pequenas rugosidades.
Para ELLINGSEN 14, quando um implante é instalado, uma série de reações acontece sobre sua superfície. O implante é exposto a uma série de diferentes íons, polissacarídeos, carboidratos e proteínas e também a células como condroblastos, fibroblastos e osteoblastos que reagem com a superfície. As reações iniciais entre os componentes do tecido e a superfície do implante governam as futuras reações e determinam a atividade biológica e, posteriormente, às respostas celulares para a superfície. A resposta do tecido depende da natureza da superfície e de suas propriedades químicas, as quais influenciam a natureza da composição subsequente do filme proteico que adsorve dentro da superfície. O autor relatou que investigações sobre a resposta osteoblástica para a síntese de hidroxiapatita apresentam diferenças de manufaturamento. Análises através de difração de raios-X apresentaram presença de íons cálcio e pequenas diferenças em impurezas por carbono, sódio, silício e alumínio. Os íons de flúor indicam aumento da atividade óssea.
Segundo STEINEMANN 4, a corrosão por buracos, bem como por fissura, é um tipo de degradação localizada do material, e tem uma ocorrência maior em ligas de alumínio, aço inoxidável e titânio. Os buracos começam a se formar em imperfeições do filme de óxido, devido à concentração de íons de cloro, no local sem que seja deslocado o oxigênio. Observa-se ainda que os buracos são nucleados em pontos que contenham traços de ferro, sendo certo que a presença deste elemento estabelece uma diferença de potencial eletroquímico. Em consequência, as ligas de titânio para emprego em implantes não devem conter ou possuir traços de ferro e, durante a fabricação e manipulação das peças, deve-se evitar a contaminação da liga com este elemento.
WIELAND et al. 10 realizaram uma revisão das técnicas usadas para a caracterização topográfica da superfície dos implantes e fundamentaram que a escolha da técnica a ser empregada está intimamente ligada à textura ou variações da superfície sendo relevantes as dimensões laterais e verticais. Salientaram ainda que, devido a distorções, artefatos de técnica, danificação da superfície e limitações de técnica os melhores métodos para a análise de superfícies rugosas são a profilometria a laser e o MEV-stereo. Primeiro, porque os mesmos alcançam o nível dimensional de interesse. Segundo, porque as técnicas não promovem contato. Assim, não destroem a superfície e terceiro, porque à luz do complexo morfológico superficial, promove grande taxa de achados na superfície que provem propriedades favoráveis para a integração óssea.
Os implantes maquinados avaliados por DAVIES7 apresentaram baixa contaminação por hidrocarbonetos com grande presença de TiO2, provendo fortes evidências de que o material é coberto por uma fina camada de óxido natural (crescimento à temperatura ambiente) e bem definido com cálculo de espessura entre 5 a 6 nm e com grande reprodutibilidade.
BINON 15 realizou uma revisão de literatura sobre as características dos implantes, incluindo sua superfície e descreveu que a interface implante-osso tem sofrido um grande desenvolvimento. A superfície original dos implantes é o titânio maquinado 5. Contudo, o mercado oferece uma variedade de modificações superficiais dos implantes tais como: TPS®, HA-Coated®, Endopore®, TiOblast®, SLA®, Osseotite ®, Osteo®, RBM®, MTX®, dentre outras. E esta variedade se deve aos específicos detalhes existentes na produção que diferenciam as superfícies.
HAYAKAWA et al. 16 realizaram um estudo in vivo para comparar a quantidade de contato ósseo em quatro diferentes tipos de superfície que eram maquinados, jateados, maquinados e com spray de fosfato de cálcio (CaP). Após 12 meses os coelhos foram sacrificados, sendo analisada histomorfometricamente e, histologicamente, a interface implante-osso. Os implantes com CaP apresentaram maiores contagens de osso sobre os implantes, concluindo que a cobertura com CaP é benéfica, favorecendo a resposta óssea na fase de cicatrização.
ORZINI et al. 17 realizaram análise de superfície de implantes de titânio maquinados versus jateados e condicionados com ácido (SLA), sendo 10 implantes usinados e 10 que apresentavam superfície SLA. O condicionamento com SLA é o jateamento de partículas Al2O3 de tamanhos entre 250-500 μm e condicionamento com ácido hidrofluorídrico 1% e ácido nítrico 30% após jateamento, para eliminar partículas de alumina, onde foi encontrada rugosidade superficial média: controle (0,75 μm) jateado e SLA (2.15 μm). Os resultados demonstraram que as superfícies apresentaram-se sem efeito citotóxico, devido à ausência de alumínio.
PLACKO et al. 8 examinou os efeitos de diferentes tratamentos (polidos, eletropolidos e jateados) sobre a morfologia e química da superfície do metal titânio comercialmente puros e liga de titânio com 6% de titânio, 4% de vanádio. A estrutura e composição das superfícies foram avaliadas usando microscopia eletrônica de varredura (MEV), microscopia de força atômica (AFM), espectroscopia por energia dispersiva (EDS), análise de microsonda Auger e espectroscopia fotoeletrônica por raios-X. Os valores de rugosidade superficial em larga escala foram, aproximadamente, idênticos para amostras jateadas e eletropolidas enquanto que, em pequena escala, amostras eletropolidas e polidas tinham valores de rugosidades aproximadamente idênticas. A composição do óxido superficial foi encontrada sendo primariamente de TiO2 em ambos os materiais e para todos os tratamentos de superfície. Vanádio não foi visto para as análises por espectroscopia fotoeletrônica de raios-X ou análise de microsonda Auger das ligas, indicando uma possível depleção superficial. O cálcio estava presente nas amostras jateadas. Cálcio e cloro foram detectados sobre amostras eletropolidas.
Descrevendo sobre a topografia da superfície, SYKARAS et al. 3relataram que está relacionada com os graus de rugosidade da superfície e com a orientação das irregularidades superficiais. Diferentes processos resultam em pouca diferença topográfica. Exemplos de métodos usados para alterar a topografia da superfície dos implantes incluem eletropolimento, decapeamento, jateamento abrasivo, borrifação de plasma, adesão superficial e fotolitografia. Existem quatro graus de Ti cp que variam principalmente quanto à quantidade de oxigênio sendo o maior, 0,4% e o menor, 0,18%. Entretanto, as propriedades do óxido não são afetadas, alterando sim as propriedades mecânicas. Traços de níquel, carbono, hidrogênio e ferro têm sido detectados. Estes adicionam estabilidade e melhoram as propriedades mecânicas e físico-químicas. O ferro é adicionado para aumentar a resistência à corrosão e o alumínio, para incrementar a elasticidade e diminuir a densidade, enquanto que o vanádio atua como um escavador de alumínio para prevenir a corrosão.
AMARANTE & LIMA 18analisaram os resultados apresentados na literatura sobre a superfície de implantes tratadas com plasma de titânio (TPS) e jateadas com partículas e tratadas com ácido (SLA). Isoladamente, a textura da superfície foi a característica mais marcante na promoção da osseointegração, sendo que há deposição óssea tanto para as superfícies lisas quanto rugosas. Entretanto, a última desempenha um papel preponderante no percentual de aposição óssea sobre a superfície do implante assim como na velocidade com que esta aposição ocorre.
JOLY & LIMA 19 realizaram uma avaliação em MEV sobre as características das superfícies dos implantes revestidos com fosfato de cálcio cerâmico, com plasma spray de titânio de um e dois estágios, com o objetivo de avaliar a fenda formada entre um abutment cônico e os implantes. Não encontrara diferença estatisticamente significativa na extensão da fenda entre os implantes.
MÜELLER et al. 20 verificaram a quantidade de contato ósseo em superfícies de titânio sem tratamento de superfície, com jateamento de AL2O3 e com biocerâmica. Os efeitos foram investigados experimentalmente em 27 coelhos após sete, 28 e 84 dias de implantação dos cilindros. Os resultados mostraram que tanto o AL2O3 quanto a biocerâmica apresentaram maior contato metal-osso do que o grupo controle sendo que, a partir do 28º dia as amostras jateadas com biocerâmica apresentaram mais osso em contato que os implantes jateados com AL2O3.
BATHOMARCO et al. 21realizaram uma análise de Ti cp usado em implantes dentais por microscopia de força atômica (AFM) com o objetivo de avaliar a morfologia, rugosidade e área de superfície de quatro amostras. Uma amostra foi constituída de superfície maquinada e as outras três apresentavam tratamento de superfície que consistia em condicionamento com banhos de ácido clorídrico, seguido de ácido hidrofluorídrico e ácido nítrico e outra amostra que sofreu jateamento de partículas de óxido de titânio (TiO2) de 50 μm de diâmetro a uma pressão de 30 psi. A última amostra recebeu os tratamentos de jateamento e condicionamento ácido. Todas as amostras receberam limpeza com acetona em banho ultrassônico por 15 minutos. Com AFM, foram adquiridas imagens da média de rugosidade superficial e a área foi calculada. Concluíram que os implantes que receberam jateamento apresentaram a superfície mais rugosa seguidos pelos que receberam condicionamento ácido. Os implantes jateados que receberam tratamento ácido apresentaram diminuição na rugosidade de superfície e o grupo controle foram os maquinados. Observaram também que as superfícies que apresentaram um aumento na área de superfície proporcionaram uma diminuição do ângulo de contato superficial. Do ponto de vista da energia superficial, os implantes que receberam jateamento com TiO2 deveriam ter mais pontos finos avaliados para os osteoblastos, o que facilitaria a aderência sobre superfícies hidrofóbicas. Entretanto, o compromisso entre a área de superfície e a molhabilidade parece ter alcançado maximização para a osseointegração.
ELIAS et al. 22apresentaram um trabalho comparando à morfologia de quatro tipos de superfície de implantes sendo as mesmas usinadas, submetidas ao condicionamento ácido, jateadas e submetidas a condicionamento ácido e anodizadas. As superfícies eram de Ti cp ASTM® grau 4 sendo que a mistura do banho de ácido continha HNO3 + HCl e o jateamento realizado por partículas de óxido de titânio e, quando seguidas de tratamento ácido, foi usado o HNO3. Quanto às análises morfológicas, estas foram realizadas em MEV e as topográficas utilizando rugosímetro. Os resultados mostraram que os implantes com as superfícies tratadas com ácido apresentaram maior homogeneidade e menor rugosidade. Os implantes jateados seguido de tratamento ácido apresentaram microcavidades com diferentes formas e tamanhos. As superfícies com tratamento eletroquímico apresentaram saliências na forma de pequenos cones. Observaram a tendência de aumento do número de células aderidas nas superfícies dos implantes com o aumento da rugosidade. Entre as superfícies analisadas os implantes com tratamento eletroquímico apresentaram características superficiais e comportamento das células mais favoráveis ao processo de osseointegração.
WENNERBERG et al. 23 analisaram in vivo e in vitro a correlação existente entre a dissociação de íons Ti com a rugosidade da superfície de implantes com superfícies modificadas por partículas e com superfícies lisas, nos períodos de 12 semanas e um ano, usando para a análise um espectroscópio de radiação X fluorescente (in vivo) e um espectroscópio de massa iônica secundária (in vitro). Ligeiro aumento de íons foi observado próximo às superfícies com maior rugosidade e com decréscimo para todas as superfícies, com o aumento de distância maior que 400 μm, nos dois períodos, podendo concluir que não houve aumento nos níveis de dissociação de íons Ti com a variação da rugosidade de superfície in vivo ou in vitro.
BRUNSKI et al. 24 relataram que as rugosidades de superfície estão relacionadas com o aumento da retenção óssea nos implantes. Os autores realizaram uma revisão sobre as diferenças encontradas entre os trabalhos que avaliavam os valores de remoção de torque para os implantes com superfícies lisas e rugosas e propuseram que, os resultados encontrados nas diversas pesquisas estavam errados, quando havia conclusão de aumento de torque para a remoção de implantes com superfície tratada, pois havia um erro quando não era considerado o aumento da área da superfície do implante devido ao seu tratamento de superfície de contato implante-osso, o que caracterizava o aumento de torque.
JARDIM JÚNIOR et al. 1 avaliaram as características de superfície de implantes Sin® desenvolvidos especialmente para pesquisas, assim como a existência de contaminação residual nos mesmos. Um total de seis mini-implantes Sin de liga de Ti cp grau II foram utilizados, todos com suas superfícies tratadas com duplo ataque ácido. A metodologia consistiu na utilização de um interferômetro analisador de superfícies tridimensionais UBM®, por meio da técnica de interferometria a laser. A seguir, para avaliar a presença de contaminantes residuais, foram retirados de seus invólucros no interior da câmara de fluxo laminar, de forma a respeitar os requisitos básicos de assepsia. Posteriormente, foi feita a transferência dos mesmos para tubos contendo caldo infuso de cérebro e coração (Difco®) suplementado com extrato de levedura (0,5%) e para tubos contendo caldo de tioglicolato (Difco®) acrescido de carbonato de cálcio, os quais foram incubados a 37°C por 72 horas e 14 dias, respectivamente. A presença de crescimento microbiano foi avaliada por determinação da absorbância do meio de cultura com o auxílio de espectrofotômetro (A380 nm). Como controle negativo, para determinação da absorbância, empregaram os próprios meios de cultura sem crescimento microbiano. Amostras também foram inoculadas em placas contendo àgar Sabouraud-Dextrose e incubadas em aerobiose, a 37°C e a temperatura ambiente, por 72 horas e 14 dias, respectivamente, para avaliar a presença de fungos leveduriformes e filamentosos nos implantes. Buscando uma completa caracterização da topografia superficial dos implantes, dados numéricos foram obtidos por meio de uma análise quantitativa, proporcionada pelos parâmetros de rugosidade considerados pelo referido estudo: Rugosidade Média (Sa) = 0,438 μm; Rugosidade Média Quadrática (Sq) = 0,567 μm; Skewness (Ssk) = 0,487; Kurtosis (Sku) = 3,68 e Altura Reduzida dos Vales (Svk) = 0,481 μm. Os valores obtidos da avaliação do crescimento microbiano pelo espectrofotômetro foram submetidos à análise estatística utilizando-se o teste de Kruskal-Wallis, com nível de significância de 5%. Independentemente da presença de microimperfeições características nestes tipos de implantes ou da topografia superficial apresentada por eles, não se evidenciou a presença de microrganismos na sua superfície.
Revisando a literatura para verificar os efeitos da topografia dos implantes sobre a integração com os tecidos mole, ROMPEN et al. 25 concluíram que, apesar da superfície rugosa apresentar melhores condições para a formação e estabilização da rede de fibrinas para a adesão celular, as superfícies maquinadas apresentam in vivo, melhor adesão ao titânio.
QAHASH et al. 26 analisaram in vitro sobre o comportamento de implantes maquinados e com superfície tratada em relação à formação de novo osso e osso nativo formado por indução através de proteína-2 morfogenética de osso humano recombinado. Os resultados demonstraram que não houve diferenças entre a densidade óssea para os dois tipos de implantes, mas, para os implantes com superfície tratada houve um grande aumento do contato osso-implante. Concluíram que o condicionamento ácido dos implantes de titânio tem um efeito positivo na osseointegração de novo osso e osso nativo e diferenças na densidade óssea parecem não ter influência neste efeito.
TAVARES et al. 27 realizaram um estudo comparativo, in vivo, sob a influência do tratamento químico da superfície na formação óssea, usando implantes MK III® que receberam um tratamento com H2SO4 e H2O2 e outros que não receberam nenhum tipo de tratamento. Realizaram a fixação dos implantes na mandíbula de cães que iriam ser sacrificados posteriormente entre três e oito semanas após o procedimento cirúrgico, para uma análise da porcentagem de contato osso-implante, o que apresentou como resultado um significante aumento de osteogênese de contato sugerindo que este tipo de superfície pode ser benéfico para a utilização de carga imediata.
Portanto, este estudo objetivou analisar qualitativamente as propriedades químicas e morfológicas da superfície de alguns implantes comercializados por diferentes empresas, no mercado brasileiro, com a intenção de qualificar morfológica e quimicamente a superfície dos implantes e o possível grau de contaminação superficial.
Metodologia
Seis implantes de titânio total puro Osseotite® (Biomet 3i – superfície tratada com ácido), Timatax® (Neodent – superfície tratada com jateamento + ácido), Máster Porous® (Conexão Sistema de Próteses – superfície tratada com ácido), Externo Laser® (Serson Implant – superfície tratada com laser), Revolution® (Sin – superfície tratada com ácido) e External Hex® (Titanium Fix – superfície tratada com jateamento) foram padronizados em relação ao seu tamanho (comprimento, diâmetro e plataforma) e, para todas as marcas, foram analisados dois implantes com superfícies modificadas por jateamento e/ou condicionamento ácido e com bombardeamento por laser.
Os implantes foram padronizados em 3.75 X 13 mm, hexágono externo e com transportador para facilitar o manuseio bem como evitar possíveis contaminações, exceto o implante Timatax® que foi transportado com broca de torque interno, pois a empresa não mais fabrica implantes com montador e, para todas as marcas, foram analisados implantes com superfícies modificadas. As amostras dos implantes foram divididas em dois grupos para a sequência de análises os quais continham um implante de cada marca. As variáveis relacionadas com a morfologia e composição química foram observadas, em duas amostras de cada um dos implantes e em três áreas pré-determinadas: cervical, meio e ápice.
Neste estudo foi usado o microscópio JEOL JSM – 6460LV da Universidade Federal do Rio de Janeiro, COPPE – Departamento de Engenharia metalúrgica, laboratório de microscopia eletrônica. O microscópio foi operado comuma voltagem de aceleração de 20 keV.
Para a reconstrução das imagens do MEV foi utilizado o software de construção de imagens Jeol Scaning Electron Microscopy. O tamanho das áreas escaneadas foi dependente do aumento e pode ser verificada pela escala nas fotomicrografias. Todas as imagens apresentavam uma resolução de 1280 x 960 pixels (pontos por polegada quadrada). As observações foram realizadas nos aumentos de 30X, 500X e 2000X.
A microssonda EDS foi utilizada, pois produz uma caracterização do biomaterial usando uma técnica analítica múltipla sendo crítica para prover informações da superfície dos biomateriais e devido a sua sensibilidade e habilidade para detectar todos os elementos com número atômico maior do que dois 7.
Para a confecção dos espectros da superfície dos implantes, primeiro foram selecionadas as áreas em menor aumento. Devido à necessidade de maior aproximação para a utilização da EDS, as análises foram realizadas nos aumentos de 500X e 2000X no mesmo campo previamente escolhido e focado para o aumento de 30X. As regiões analisadas pela EDS foram as mesmas avaliadas morfologicamente.
Foi então realizada a marcação de pontos em áreas que se apresentavam diferentes do padrão do campo visualizado. Foi tentado o uso de Anova, que consiste em um procedimento paramétrico utilizado para verificar se as médias variam ao longo dos grupos analisados. Os pressupostos para a realização deste teste são: normalidade (os dados devem estar distribuídos segundo a curva normal); homocedasticidade (variâncias iguais ao longo dos grupos) e os tamanhos dos grupos devem ser próximos. Nos dados verificados não foi observada normalidade por meio das provas de Shapiro-Wilk. Entretanto, a violação deste pressuposto não impossibilitou o uso de Anova, pois a homocedasticidade é um pressuposto mais importante e esta foi encontrada na amostra utilizando-se o teste de Levene (verificação se as variâncias são iguais ao longo dos grupos testados). Entretanto, no uso de Anova não foi encontrada significância, mostrando que não houve evidências para rejeitar a hipótese de que alguma média fosse estatisticamente diferente das demais.
Desta forma, tentou-se constatar alguma diferença existente entre os grupos utilizando outras provas estatísticas não paramétricas. Inicialmente, foi utilizada a prova de Kruskal-Wallis para identificar se alguma mediana de um dos grupos se diferenciava das demais e também não foi obtida significância neste teste. Logo após, aplicou-se a prova de Mann-Whitney para verificar diferenças das medianas entre grupos, comparando par a par, e Kolmogorov-Smirnov para efetuar comparações de dois a dois grupos. Na prova de Kolmogorov-Smirnov foi possível identificar apenas uma diferença ao nível de 0,07 (p = 0,07) entre os implantes Externo Laser® (Serson Implant) e Timatax® (Neodent) frente aos demais utilizados no estudo.
Resultados
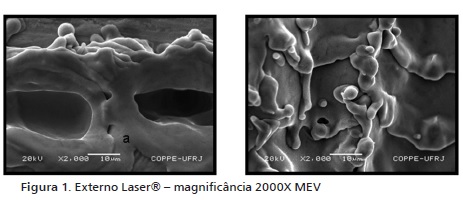
Sobre a morfologia superficial em MEV, foi observado presença de cavacos de usinagem, partículas, ranhuras, alterações na superfície das roscas e de coloração, características topográficas e outras de diversos tamanhos sobre a superfície de alguns implantes sugerindo diferenças entre os processos de fabricação dos implantes comercializados no Brasil (figuras 1 e 2).
Cada implante exibiu características próprias de superfície que estão ligadas aos diferentes processos de fabricação, como: tratamentos de superfície e processos de limpeza, esterilização e empacotamento.
Como característica topográfica marcante, utilizando a observação visual das fotomicrografias de superfície, para cada tipo de implante foi observado: os implantes Revolution ®, Osseotite® e Máster Porous® apresentaram uma superfície com padrão poroso de aproximadamente 1 a 10 μm de largura (tamanho dos poros), bem padronizado e com poucas ranhuras e que o implante Máster Porous® apresentou áreas sem porosidades.
A superfície dos implantes Timatax® e External Hex® possuem áreas com características semelhantes na rugosidade. Uma grande diferença foi encontrada nos implantes Externo Laser® que apresentam um tratamento de superfície por bombardeamento a laser (segundo fabricante), apresentando poros somente na região cervical onde temos o início da aplicação do laser, estes com tamanhos maiores do que 10 μm; partículas espalhadas ao redor foram encontradas devido à refundição causada pelo laser visto que a sua superfície tem um aspecto escovado em um menor aumento e deformado sem um padrão de poros definidos em um maior aumento.
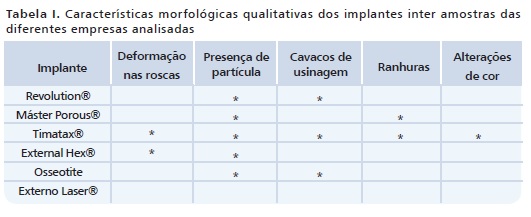
Após compilação dos resultados, foram apresentadas na Tabela I as características morfológicas qualitativas dos implantes, interamostras das diferentes empresas analisadas, no que tange a alterações morfológicas na superfície dos implantes dentários comercializados no Brasil.
Dentre as alterações mais frequentes, encontram-se a presença de partículas orgânicas e inorgânicas, as quais foram encontradas em cinco amostras e em todas as regiões, exceto nos implantes Externo Laser® que apresentaram um tratamento físico de superfície por bombardeamento a laser. As outras marcas analisadas apresentaram tratamento de superfície por jateamento de partículas e/ ou condicionamento ácido o que poderia ser a possível causa da presença de partículas remanescentes.
Quanto à análise química (EDS), após análise de 13 pontos, em oito áreas propostas, em dois implantes Osseotite®, foi encontrada Ca, C e O no meio e ápice das amostras e Cl na região cervical, contudo a grande maioria da superfície é constituída de Ti. Deve-se observar que na região cervical, o implante não apresenta tratamento de superfície como nas demais regiões e, no entanto, o mesmo apresenta contaminações por elementos diferentes nestas diferentes superfícies.
Nos implantes Revolution®, após análise de 10 pontos, em seis áreas propostas, encontrou-se na região cervical o C, Cl e o P e no meio foram identificados os elementos C, Na, O e Ca. Para todos os pontos analisados e que apresentavam elementos contaminantes, sendo estes oriundos de partículas na superfície, exceto para os identificados no meio da amostra que estavam dentro de uma cratera na superfície. Por outro lado, é importante salientar que o Ti foi o elemento mais contado para a análise proposta.
Quando foram analisados 11 pontos, em setes áreas propostas nos implantes Timatax®, encontrou-se (cervical e ápice) resíduos de C (cervical), S, O, Al e Si (ápice), mas a grande maioria da superfície foi constituída de Ti. Cabe salientar que todos os elementos contaminantes constatados nas amostras foram identificados em partículas que estavam sobre a superfície. Neste caso há uma diferença marcante dentre os outros implantes analisados, pois foi encontrado Al na região cervical a qual é isenta de tratamento de superfície. Já na região tratada (ápice) o mesmo não foi encontrado sendo que, os elementos identificados nesta região foram o C, O, Si e o S.
Nos implantes Externo Laser® foram analisados oito pontos, em quatro áreas, não sendo encontrado nenhum contaminante superficial, sendo o Ti o único elemento. Devido ao padrão do tratamento e os resultados obtidos, evidenciando as propriedades químicas desta superfície, foi realizado um número menor de pontos e áreas, pois os mesmos já demonstravam constituintes de superfície, as quais não apresentavam alterações visuais do padrão.
Após análise de 11 pontos, em seis áreas propostas dos implantes Máster Porous®, foram encontradas partículas de Ca, Co, O (cervical) e C, O, Na, Cl, e K (ápice), contudo, as demais regiões observadas apresentaram a presença de Ti. Contudo, todos os contaminantes foram observados no grupo I sendo que, o grupo II apresentou-se livre de contaminantes nos pontos marcados.
Foram analisados 13 pontos, em seis regiões, sendo duas de cada terço proposto dos implantes External Hex®, sendo encontrando no meio do implante Al e C; no ápice foi encontrado além de C e O e, na cervical C, Si, S, Cl e K; entretanto a grande maioria da superfície continha Ti. Uma das características observadas nesta marca de implante foi a constatação de Al somente nas regiões tratadas e a EDS apontou sua presença tanto sobre partículas quanto fora delas. Já os outros elementos identificados estavam na região cervical, exceto o C, em uma região em que não havia sido feito tratamento superficial, mas que continha partículas, sendo que foi evidenciada, nestas partículas, a presença dos outros elementos supracitados.
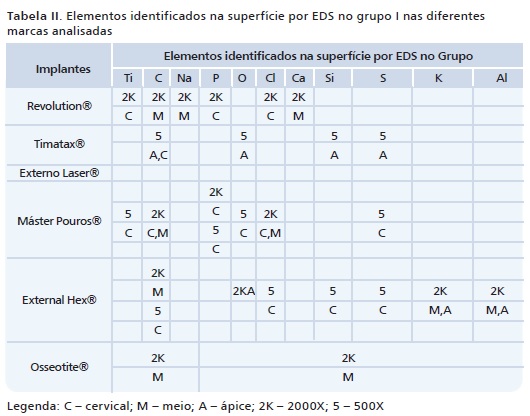
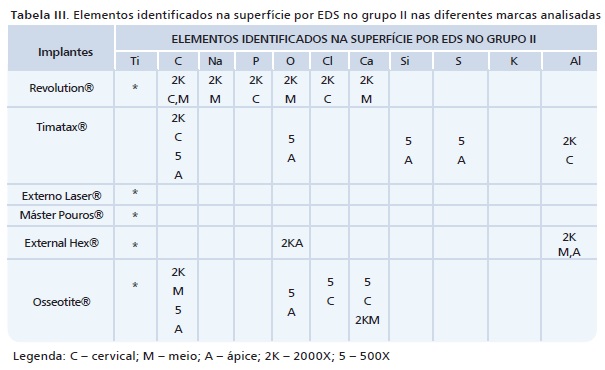
Após a análise dos espectros produzidos pela sondagem por dispersão de elétrons, nos pontos marcados, foram determinadas as Tabelas II e III que apresentam todos os elementos identificados na superfície das amostras estudadas dos grupos I e II, respectivamente. Pôde-se observar que além do Ti e do O, o C foi o segundo elemento com maior incidência entre as amostras, seguido pelo P, Cl e o Na. O S, a Si e o Al foram identificados apenas em duas superfícies (Timatax® e External Hex®), o mesmo acontecendo com o K (Máster Porous® e Timatax®).
Discussão
Na década de 60, iniciou-se a era da Implantodontia odontológica moderna. Naquele tempo, estudos por microscopia in vivo na busca do entendimento de como os tecidos ósseos inicialmente cicatrizavam-se, realizados por Bränemark e colaboradores utilizando uma cânula de titânio, deu vida aos conceitos da osseointegração 5. Desde então, vem se estudando sobre os fenômenos que participam das interações entre os tecidos vivos e os implantes de titânio 3,4,6,7. Uma apropriada resposta tecidual frente ao biomaterial depende de diversos fatores que envolvem tanto os implantes como a técnica cirúrgica e as respostas promovidas pelo receptor 5,7. Em relação ao titânio, devem-se considerar os aspectos que tangem sua composição química bem como as propriedades inerentes da sua superfície que, em última análise, promoveram as condições finais para que os primeiros eventos entre o biomaterial e o hospedeiro, resultem no sucesso da terapia com implantes que é a osseointegração 5.
O titânio é o material de escolha na terapia com implantes devido à grande reatividade. Está propriedade lhe confere a formação de um óxido em sua superfície que é extremamente estável e compatível quando em contato com o ar, água ou qualquer outro eletrólito. Este óxido forma-se espontânea e quase instantaneamente e de forma muito reproduzível 3,4,10. O óxido, além de denso é extremamente resistente, protegendo a superfície do implante contra ataques químicos (corrosão). Então, a interface implante-tecido é governada pela camada de óxido e não pelo metal em si, concluiu-se que, para a osseointegração o que importa é a constituição da camada de óxido e não o metal 4,7.
Após a escolha de uma liga de titânio, os fatores que irão influenciar as propriedades na camada de óxido, do produto final que será comercializado tais como espessura, composição química e microestrutura dependerão da pressão, velocidade de usinagem, tratamento de superfície, limpeza, esterilização, acondicionamento e estocagem 3,4,5,7,9,14.
Alguns elementos têm sido adicionados para a melhoria dos comportamentos físico-químicos e mecânicos da liga. Contudo, os mesmos podem levar a contaminação da camada final de óxido sobre a superfície, alterando o comportamento celular de forma positiva ou negativa 3,11.
Esta pesquisa foi elaborada com o objetivo de avaliar as possíveis diferenças morfológicas e a presença de possíveis contaminantes orgânicos e inorgânicos, em seis diferentes marcas de implantes mais comercializados no mercado brasileiro e com superfícies modificadas visto que, diversos autores têm demonstrado a relevância das características superficiais da camada de óxido de titânio para a osseointegração 3-8,11.
Atualmente, existem vários métodos para a análise que empregam interação entre a superfície do material analisado e os conceitos relacionados à física quântica. O método a ser escolhido deve responder aos objetivos a que este trabalho se propõe que são: 1) analisar o gráfico da composição química da superfície e determinar sua possível contaminação devido ao seu processamento; 2) avaliar as possíveis alterações morfológicas nas superfícies devido aos tratamentos modificadores nelas realizados.
A escolha pelo uso do MEV/EDS se deu tendo em vista ser esta a ferramenta mais apropriada para a avaliação morfológica, bem como para a aquisição de dados para a caracterização química das superfícies analisadas. Através do MEV, foram realizados aumentos com magnificações de 30X, 500X e 2000X habilitando a identificação dos padrões morfológicos de cada superfície, bem como suas características individuais, como: presença de partículas, ranhuras, alterações na cor, alterações no acabamento das roscas, presença de cavacos 3,8, visto que diferentes processos resultam em pouca diferença topográfica e que esta necessita de pelo menos duas dimensões para ser medida9. Além disso, sem um processo padrão de análises é impossível comparar os valores de um estudo com o outro 23.
Apesar de um único método não ser suficiente para a caracterização completa de uma superfície, a microssonda EDS é o instrumento mais indicado para rotina de microanálises, particularmente no caso da determinação de elementos menores ou em situações em que se queira maior resolução espectral, sendo que a mesma consegue uma análise de até 5μm de profundidade na superfície.
As seis marcas de implantes utilizadas foram padronizadas em relação ao seu tamanho (comprimento, diâmetro e plataforma) e, para todas as marcas, foram analisados implantes com superfícies modificadas por jateamento e/ ou condicionamento ácido e com bombardeamento por laser. Os implantes foram padronizados em 3,75 X 13 mm, hexágono externo e para todas as marcas foram analisados implantes com superfícies modificadas. As variáveis relacionadas com a morfologia e composição química foram observadas em duas amostras (grupo I e grupo II) de cada um dos implantes e em três áreas pré-determinadas foram: cervical, meio e ápice.
O número de amostras (n = 2) de cada implante usado nesta pesquisa, sendo que um número de amostras maior não foi aplicável neste estudo, pois há diferença entre cada amostra em relação aos contaminantes e características morfológicas.
As diferentes marcas de implantes avaliadas mostraram diferenças morfológicas superficiais, sendo que intragrupos apresentaram o mesmo padrão, mas como não se tem informações suficientes em relação à técnica usada para criar as rugosidades superficiais das amostras comercializadas 3, foi analisada qualitativamente e relacionar possíveis características morfológicas e químicas encontradas em suas superfícies.
No que tange às características morfológicas, a presente análise demonstrou que todas as superfícies apresentaram alguma característica que as tornava rugosa devido a específicos detalhes de produção 22 e, segundo AMARANTE & LIMA 18, essa desempenha um papel preponderante no percentual de aposição óssea sobre a superfície do implante assim como na velocidade com a qual esta aposição ocorre 24, apesar de ROMPEN et al.25 relatarem que, in vitro, as superfícies lisas apresentaram melhor adesão celular. Para QAHASH et al. 26, não há diferenças entre a densidade óssea para as superfícies lisa e rugosa.
Segundo alguns autores 8,11,12,22, os estudos com as superfícies rugosas na formação da camada de óxido e na agregação celular não apresentam alterações desta e nem implicações biológicas e não se verificou aumento nos níveis de dissociação do Ti 23.
Uma característica marcante do estudo foi em relação aos implantes SERSON que apresentaram um tratamento de superfície por bombardeamento a laser (segundo fabricante), apresentando poros somente na região cervical, onde temos o início da aplicação do laser, estes com tamanhos maiores do que 10 μm; partículas espalhadas ao redor foram constatadas devido à refundição causada pelo laser, sendo que a sua superfície tem um aspecto escovado em um menor aumento e deformada sem um padrão de poros definidos em um maior aumento configurando uma superfície mais lisa do que rugosa 8,27.
No entanto, nos demais implantes analisados foram observadas a presença de partículas, na superfície, nos três aumentos e em todas as regiões o que sugere deficiências nos processos de limpeza e esterilização dos mesmos 7. As partículas se apresentaram de diversos tamanhos, mas pôde-se observar uma maior frequência na região cervical das amostras, o que se acredita que os tratamentos de superfície ajudam a eliminar contaminantes, sendo mais evidenciado nos implante Externo Laser®, os quais receberam um tratamento físico, não apresentando alterações no padrão morfológico e nem contaminações superficiais por possíveis produtos de limpeza.
Alterações de acabamento nas roscas bem como ranhuras foram repetidamente exibidas nos implantes Titamax® nas regiões cervical e meio e External Hex®. External Hex® somente na cervical nos três aumentos e Cavacos de usinagem foram observados nos implantes Revolution®, Osseotite®, Máster Porous® e Titamax® no menor e no maior aumento na região cervical. Estas alterações morfológicas indicam deficiências no processo de usinagem dos implantes, que podem ser devido à velocidade de usinagem, qualidade do equipamento ou até falta de manutenção dos mesmos, demonstrando que os procedimentos de tratamento superficial ajudam na limpeza e homogeneidade da superfície 8,11.
Foi observado também alteração de coloração da superfície no implante Titamax® no menor aumento. Este achado pode indicar aquecimento no momento de usinagem dos implantes que pode comprometer as características do óxido de titânio, levando às modificações na interface que podem comprometer a osseointegração 4,5.
Como já esperado, as superfícies de implantes Ti cp deveriam conter apenas Ti em sua superfície. Por sua vez, os implantes sofrem processos de usinagem, tratamento, limpeza, embalagem, esterilização e estocagem que poderão influenciar na qualidade dos elementos componentes da superfície dos implantes que serão comercializados para o uso clínico 3,7,8,11. Em relação à presença de elementos químicos na superfície foi possível afirmar que o Ti é o elemento majoritariamente presente nas superfícies analisadas. Todavia, outros elementos contaminantes também foram identificados nas amostras: C, Na, P, O, Cl, Ca, Si, S, K e Al.
A presença do oxigênio nas amostras se deve à corrosão instantânea das superfícies de Ti cp, sendo que sua presença caracteriza a formação de TiO2, óxido este que governa o comportamento químico inerte dos implantes e promove as condições biológicas ideais para o fenômeno da osseointegração e, em última análise, não correspondem como elementos contaminantes 3,4,5,7,8,22.
Já o carbono aparece como um contaminante orgânico que pode ter sido adquirido do ar, no momento da exposição dos implantes para o preparo das amostras ou por falhas na limpeza, esterilização e empacotamento dos mesmos, pois o Ti cp não apresenta este elemento em sua constituição e, mesmo quando identificado, apresenta-se como partículas sobre a superfície das amostras 3,8.
Realizando uma análise intramarcas, foi possível afirmar que os implantes Externo Laser® foram os únicos que não apresentaram contaminantes superficiais, para as análises por EDS das amostras investigadas, pós-tratamento físico da superfície, bombardeamento a laser, conforme fabricante, confirmando que o tipo de tratamento de superfície interfere no padrão químico final da camada superficial dos implantes, quando comparado com as outras marcas de implante que receberam tratamento por jateamento de partículas e/ou condicionamento ácido 9,11,14. Constataram-se também diferenças nos espectros das regiões marcadas entre implantes das outras marcas.
Os implantes External Hex® foram os que apresentaram maior número de contaminantes superficiais: C, O, Cl, Si, Ca, S, K e Al. Houve uma diferença entre os implantes do grupo I e II onde, o grupo I apresentou baixas contagens C, Si, S, Cl e K na região cervical e o grupo II, na mesma região, não apresentou elementos contaminantes, região esta que não recebeu tratamento superficial, indicando deficiência na padronização dos processos de limpeza. A presença destes elementos informa que os implantes receberam banhos ácidos para a limpeza da superfície e que estes não foram devidamente removidos. Comparando as regiões do meio e cervical entre os dois grupos verificou-se que o Al e O estiveram presentes nos dois grupos e o Ca no grupo II; contudo, este grupo apresentou elevada contagem de escaneamento para o Al no ápice do implante. Estes achados corroboram as características morfológicas superficiais desta marca de implante que apresenta superfície rugosa com características de jateamento e que, com a identificação do Al nas regiões tratadas nos levam a crer que, o mesmo sofreu um tratamento por jateamento com partículas de óxido de alumínio, pois o espectro da EDS foi relativo às partículas sobre a superfície. Isto indica deficiências nos processos de limpeza. Out ra possibilidade para a presença do Al seria em relação aos elementos constituintes que só poderíamos identificar tal elemento se o metal utilizado não fosse Ti cp e sim uma liga com Al em sua constituição (4). O cálcio apresentou baixas contagens de escaneamento e sua presença pode ser consequência dos processos de limpeza devido à precipitação do mesmo, promovida pelo uso de detergentes e algum tipo de veículo contaminado pelo cálcio, ou até mesmo pela esterilização 8,14.
A análise dos resultados obtidos para as amostras dos implantes Titamax® mostrou variada contagem de elementos contaminantes em sua superfície. Os elementos encontrados foram: C, O, Si, S, Al, Si e S. O. O alumínio foi o único contaminante identificado no grupo II, na região do cervical, sendo todos os outros identificados no grupo I. A Si e S foram identificados no espectro da EDS da região apical. Tais evidências somadas com os resultados das características morfológicas dos implantes Titamax® sugerem que estes implantes receberam um tratamento de superfície por jateamento com partículas a base de Al e Si, somado a condicionamento ácido a base de S. Os espectros apontam também para problemas na limpeza final dos implantes devido à contaminação apical e falta de controle das áreas que receberam o jateamento, visto que a região cervical é lisa.
Os implantes Revolution® apresentaram também grande espectro de elementos contaminantes superficiais que correspondem aos elementos C, Na, O, Ca, P, Cl. Na região cervical, isenta de tratamento superficial foi identificado o C, Cl e P. A característica morfológica lisa desta região e a identificação do Cl e o P sugerem que a sua presença se deve a problemas na completa remoção de agentes ácidos na limpeza final das amostras analisadas, sendo que a EDS para esta identificação foi realizada sobre partículas na superfície. Porém, na região do meio foram identificados os demais elementos Na e Ca, os quais são também identificados em outros trabalhos, quando os implantes são submetidos à esterilização por autoclave ou quando são submergidos em água 14. Tais características podem indicar, também, deficiências na qualidade dos fluidos detergentes de enxágue dos implantes. Estes poderão precipitar de forma insolúvel tais elementos. Outra possibilidade seria processos de anodização destas superfícies. Sendo assim, poderia verificar com mais frequência a presença de partículas de Ca e P, o que não aconteceu 22.
O espectro produzido pelas análises por EDS para os implantes Máster Porous apresentaram uma grande variedade de elementos contaminantes: C, O, Cl, Na, K, Ca e S. No grupo II, somente o C foi identificado como contaminante. Já no grupo I os pontos que apresentaram os elementos que não eram Ti, compreendiam áreas onde foi aplicada a EDS em partículas presentes no campo. Isto caracteriza uma deficiência nos processos de limpeza e falta de qualidade dos fluidos enxaguantes, esterilização ou até mesmo imersão em água do implante 14; outra possível causa aventada seriam processos de anodização destas superfícies, mas neste caso, poderíamos verificar com mais frequência a presença de Ca. Há diferença entre o tipo de contaminante em relação à região analisada, pois onde os elementos encontrados em regiões tratadas (ápice: Na, Cl, K) diferem dos encontrados na região que não sofreu tratamento superficial (cervical: Ca). O C que foi evidenciado em ambas as regiões pode ter sido adquirido por contato com o ar quando da abertura dos implantes ou ser contaminação orgânica do processamento 3.
Por fim, os implantes Osseotite® receberam análise por sonda EDS conforme as amostras das marcas anteriores identificando- se: Cl, C, Ca e P. Verificou-se que no grupo I o único contaminante além do C foi o Ca na região do meio do implante. Já no grupo II, verificou-se que na região cervical, a identificação de um espectro para o Cl. A presença deste elemento em uma superfície lisa caracteriza deficiências de limpeza da amostra desse grupo. Nas outras regiões meio e ápice, as quais receberam tratamento superficial, foram identificados: Ca, C, P, e o CL em partículas.
A composição química irá promover diferentes reações no meio circundante. A constelação química da superfície oferece diferenças de bulk do material previsto para métodos de preparação e para impurezas aprisionadas na superfície 9,11.
A presença de pelo menos um dos elementos Na, Ca e K, na superfície das amostras estudadas, abrem uma janela para a pesquisa sobre as condições de processamento industrial dos implantes e suas reais influências na química superficial.

Conclusão
Com base nos resultados obtidos em MEV e EDS pode-se concluir que: nas amostras analisadas houve presença de impurezas, após modificações na superfície; o tratamento de superfície influenciou a morfologia da superfície e na presença de contaminantes; houve diferenças morfológicas entre implantes de diferentes marcas; todos os implantes analisados apresentaram partículas em sua superfície, exceto o Externo Laser®, que somente apresentou Ti; nas amostras analisadas a presença de titânio foi sempre observada; os implantes Externo Laser® apresentaram morfologia superficial compatível a uma superfície lisa; os implantes Titamax® apresentaram o maior espectro de elementos contaminantes; o carbono e o cloro foram os elementos mais identificados nas diversas superfícies; o alumínio só foi identificado na superfície dos implantes External Hex® e Titamax®; o implante Osseotite® apresentou contaminantes.
Referências
1. JARDIM JÚNIOR, E. G. et al. Características da topografia superficial e de contaminação microbiana de implantes Sin® desenvolvidos para pesquisa. Innov. Implant. J. 2006; 1 (2): 25-9. [ Links ]
2. STEINEMANN, S. G. The Insult of Foreign Body. Europ. Cells Materials. 2000; 1 (1).
3. SYKARAS, N. et al. Implant Materials, Designs, and suface Topogrphies: Their Effect on Osseointegration. A Literature Review. Int. J. Oral Maxillofac. Implants. 2000; 15 (5): 675-90.
4. STEINEMANN, S. G. Titanium – the material of choice? Periodontology 2000. 1998; 17: 7-21.
5. BRÄNEMARK, P. I. Surface Properties and Osseointegration. In: BRÄ- NEMARK, P. I. et al. The osseointegration Book: from Calvarium to Calcaneus. Berlin, 2005; 5.
6. BRUNSKI, J., PULEO, D., NACI, A. Biomaterials and Biomechanics of Oral and Maxillofacial Implants: Current Status and Future Developments. Int. J. Oral Maxillofac. Implants. 2000; 15 (1): 15-46.
7. DAVIES, J. E. Bone Engineering- Workshop, Toronto, Canada; 1999.
8. PLACKO, H. E. et al. Surface characterization of titanium-based implant materials. Int. J. Oral Max. Implant. 2000; 15 (3): 355-63.
9. WENNERBERG, A., ALBREKTSSON, T. Suggested Guidelines for Topographic Evaluation of implant Surface. Int. J. Oral Maxillofac. Implants. 2000; 15: 331-4.
10. WIELAND, M. et al. Measurement and evaluation of the chemical composition and topography of titanium Implant Surface. In: DAVIS, J. E. Bone Engineering – Bone Engineering Workshop. Toronto, Canada. 1999; (14): 165-82.
11. MAETZU, M. A., ALAVA, J. I., GAY-ESCODA, C. Ion implantation: surface treatment for improving the bone integration of titanium and Ti6Al4V dental implants. Clin. Oral Impl. Res. 2003; 14: 57-60.
12. CONTERNO, G. et al. Surface treatment on biomaterials: acid etching on titanium surfaces. 19th European Conference on Biomaterials. Sorrento: Italy 2005; 11-5.
13. PIMENTA, J., CASTRO, F. Chemical modification of pure titanium surfaces for oral implant. Implant Dent. 1990; 8: 86-9.
14. ELLINGSEN, J. E. Surface configuration of dental implants. Periodontology 2000. 1998; 17: 36-46.
15. BINON, P. P. Implants and components: Entering the New Millennium. Int. J. Oral Maxillofac. Implants. 2000; 15 (1): 76-94.
16. HAYAKAWA, T. et al. Effect of surface roughness and calcium phosphate coating on the implant/bone response. Clin. Oral Impl. Res. 2000; 11: 296-304.
17. ORZINI, G. et al. Surface Analysis of machined Verssus Sandblaster and Acid-etched titanium Implants. JOMI. 2000; 15 (6): 779-84.
18. AMARANTE, E. S., LIMA, L. A. Otimização das superfícies dos implantes: plasma de titânio e jateamento com areia condicionado por ácido - estado atual. Pesqui. Odontol. Bras. 2001; 15 (2): 166-73.
19. JOLY, J. C., LIMA, A. F. M. Characteristics of implant surface and implant abutment gap in two-and one-stages systems. J. Appl. Oral Sci. 2003; 11 (2): 107-13.
20. MÜELLER, W. D. et al. Evaluation of the interface between bone and titanium surfaces being blasted by aluminium oxide or bioceramic particules. Clin. Oral Impl. Res. 2003; 14: 349-56.
21. BATHOMARCO, R. V. et al. Atomic force Microscopy analysis of different surface treatments of Ti dental implant surfaces. Applied Surface Science. 2004; 23: 29-34.
22. ELIAS, C. N. et al. Diferentes superfícies dos implantes Dentários. In: III Congresso Latino Americano de Órgãos Artificiais e Biomateriais Campinas. 2004.
23. WENNERBERG, A. et al. Titanium release from implants prepared with different surface roughness. An in vitro and in vivo study. Clin. Oral Impl. Res. 2004; 15 (5): 505-12.
24. BRUNSKI, J. B. et al. Transfer of Mechanical Load Across the interface. In: BRÄNEMARK, P. I. et al. The Osseointegration Book: from Calvarium to Calcaneus. 2005; (10): 209-49.
25. ROMPEN, E. et al. The effect of material characteristics, of surface topography and of implant components and conections on soft tissue integration: a literature review. Clin. Oral Impl. Res. 2006; 17 (2): 55-67.
26. QAHASH, M. et al. Surface-Etching enhances Titanium Implant Osseointegration in Newly formed (rhBMP-2-Induced) and Native Bone. Int. J. Oral Maxillofac. Implants. 2007; (22): 472-77.
27. TAVARES, M. G. et al. Treatment of a commercial, machined surface titanium implant with H2SO4/H2O2 enhances contact osteogenesis. Clin. Oral Impl. Res. 2007; (18): 452-58.
 Endereço para correspondência:
Endereço para correspondência:
João Galan
Jr. Rua José Miguel Santos, casa 4 - Jacumã, Conde
Paraíba/PA, Brasil – CEP: 58322-0000
e-mail: galanjr.joao@gmail.com
Recebido: 16/05/2013
Aceito: 18/06/2013