Serviços Personalizados
Artigo
Links relacionados
Compartilhar
RPG. Revista de Pós-Graduação
versão impressa ISSN 0104-5695
RPG, Rev. pós-grad. vol.17 no.1 São Paulo Jan./Mar. 2010
ARTIGOS CIENTÍFICOS
Avaliação da diluição do DNA extraído de material parafinado para amplificação em PCR
Evaluation of DNA dilution extracted of paraffin-embedded material for PCR amplification
LEANDRO TOYOJI KAWATA I; NEIVIO JOSÉ MATTAR II; JOSÉ FERNANDO GARCIA III; EDER RICARDO BIASOLI IV; FÁBIO DAUMAS NUNES V; GLAUCO ISSAMU MIYAHARA VI
I Professor Doutor do Curso de Odontologia do Centro Universitário de Lavras (UNILAVRAS) – Lavras/MG
II Médico Patologista do Instituto de Patologia de Araçatuba – Araçatuba/SP
III Professor Adjunto do Departamento de Apoio, Produção e Saúde Animal da Faculdade de Odontologia e Medicina Veterinária de Araçatuba – Araçatuba/SP
IV Professor Adjunto do Departamento de Patologia e Propedêutica Clínica da Faculdade de Odontologia de Araçatuba da Universidade Estadual –Júlio de Mesquita Filho– (UNESP) – Araçatuba/SP
V Professor Associado do Departamento de Estomatologia da Faculdade de Odontologia da Universidade de São Paulo (FOUSP) – São Paulo/SP
VI Professor Adjunto do Departamento de Patologia e Propedêutica Clínica e Vice-Supervisor do Centro de Oncologia Bucal da Faculdade de Odontologia de Araçatuba da Universidade Estadual –Júlio de Mesquita Filho– (UNESP) – Araçatuba/SP
RESUMO
Introdução: Alguns fatores, como a presença de substâncias inibidoras e degradação do DNA, podem contribuir para a falha na detecção de genes, através da reação em cadeia da polimerase (PCR), a partir de DNA extraído de material parafinado. A diluição do DNA frequentemente pode reduzir o número de inibidores e contaminantes e ainda assim conter DNA suficiente para a amplificação em PCR. Objetivo: Avaliar a influência da diluição de soluções de DNA extraído de material parafinado na amplificação por PCR do gene β-globina humana. Material e método: Foram utilizados 30 blocos parafinados de carcinomas epidermoides de orofaringe referentes a pacientes diagnosticados e tratados no Centro de Oncologia Bucal da FOA-UNESP. A extração do DNA foi realizada com o sistema QIAamp DNA minikit (Quiagen). O DNA obtido foi quantificado e avaliado quanto à pureza por espectrofotometria. Dois grupos foram formados com diferentes quantidades de DNA, sendo que o Grupo I foi constituído pelo DNA originalmente extraído e o Grupo II com o mesmo DNA, porém diluído com adição de água ultrapura. Foi realizada a PCR utilizando-se oligonucleotídeos iniciadores para β-globina. Resultados: No Grupo I, 33,33% das amostras foram positivas para o gene β-globina, enquanto no Grupo II, 23,33% foram positivas. Conclusão: Neste estudo, a diluição do DNA extraído de material parafinado não alterou estatisticamente a quantidade de amostras positivas por PCR para o gene β-globina, embora os resultados obtidos sugiram que esta seja uma das formas de aumentar a eficácia do método de amplificação por PCR.
Descritores: Reação em cadeia da polimerase. Inclusão do tecido. Carcinoma de células escamosas.
ABSTRACT
Introduction: Several reasons may lead to the failure of polymerase chain reaction (PCR) using DNA purified from paraffin-embedded materials: presence of inhibitors and degradation of target DNA. DNA dilution will often reduce the concentration of potential inhibitors and still contain enough DNA to allow PCR amplification. Objective: To evaluate the dilution influence of DNA purified from paraffin-embedded materials on β-globin PCR amplification. Material and Method: Paraffin-embedded blocks from 30 patients with oropharynx squamous cell carcinomas, diagnosed and treated at the Oral Oncology Center were selected. DNA extraction was performed using QIAmp minikit (Quiagen). DNA was quantified and evaluated for purity by spectrophotometer analysis. Two groups were formed with different amounts of DNA: group I had the originally extracted DNA and group II had the same DNA, however diluted with ultrapure water addition. PCR was performed in both groups using oligonucleotides for human β-globin gene. Results: For Group I, amplification of the β-globin gene sequence was successful in 33.33% of the samples and for Group II, in 23.33%. Conclusion: Dilution of the DNA extracted of paraffin-embedded materials did not modify statistically the amount of positive samples β-globin gene amplified in PCR, although the results suggest that this is a way to increase the method for efficacy amplification of PCR.
Descriptors: Polymerase chain reaction. Tissue embedding. Carcinoma, squamous cell.
Introdução
Com o avanço técnico-científico da biologia molecular, várias técnicas têm sido disponibilizadas nos últimos anos, sendo que, com o auxílio da técnica da reação em cadeia da polimerase (PCR), a partir de 1985, ocorreu uma revolução na análise de ácidos nucleicos. Com isso, os materiais de arquivos tornaram-se uma importante fonte de pesquisa de DNA pela patologia molecular. Soma-se a este fato o inestimável valor desse tipo de análise para estudos epidemiológicos retrospectivos8.
Devido aos exames histopatológicos rotineiramente realizados, os tecidos parafinados são as principais fontes de material biológico de arquivo. No entanto, a dificuldade em detectar o DNA pela PCR em espécimes fixados em formol e incluídos em parafina tem sido relatada22.
Alguns fatores podem contribuir para a falha na realização da PCR com DNA extraído de material parafinado, como a presença de substâncias inibidoras da enzima DNA polimerase1,7,18 e a degradação do DNA10,18, que pode ocorrer devido ao tempo entre a remoção cirúrgica do tecido e a fixação, tipo de fixação e duração da fixação9.
A diluição do DNA pode reduzir o número de inibidores e contaminantes numa reação e, ainda assim, manter DNA suficiente para a amplificação por PCR24.
Este trabalho tem como objetivo avaliar a influência da diluição do DNA extraído de material parafinado na amplificação pela PCR do gene da β-globina humana.
Material e Métodos
Este trabalho foi aprovado pelo Comitê de Ética em Pesquisa da Faculdade de Odontologia de Araçatuba (FOA-2006-01177). Neste estudo, foram utilizados 30 blocos parafinados de carcinomas epidermoides de orofaringe, originalmente fixados em formol a 10%, referentes a pacientes diagnosticados e tratados no Centro de Oncologia Bucal da Unidade Auxiliar da Faculdade de Odontologia de Araçatuba, UNESP.
Foram obtidos de três a seis cortes histológicos dos blocos de acordo com o seu tamanho, de modo que o material coletado pesasse aproximadamente 25 mg sem excesso de parafina. Este material foi acondicionado em tubos de polipropileno de 1,5 mL. Aos tubos foram adicionados 1.200 mL de xilol, sendo os mesmos agitados em vórtex durante 1 minuto e centrifugados à velocidade de 14.000 rotações por minuto (rpm) durante 5 minutos. O sobrenadante foi desprezado e adicionaram-se 1.200 mL de álcool absoluto. Os tubos foram agitados em vórtex durante 1 minuto e centrifugados à velocidade de 14.000 rpm durante 5 minutos. O álcool foi removido com pipeta e os tubos permaneceram abertos durante 10 minutos na estufa a 37ºC para evaporação completa do álcool. Em seguida, foi realizada a extração do DNA com o sistema de extração QIAamp DNA minikit (Quiagen®) conforme instrução do fabricante, obtendo-se volume final de 100 mL de solução de DNA purificado.
A quantidade e a pureza do DNA genômico foram determinadas pela densidade óptica em espectrofotômetro (NanoDrop® ND- 1000 UV-VIS). Neste momento, foram formados dois grupos, sendo que no Grupo I foi utilizado o DNA originalmente extraído e, no Grupo II, o mesmo DNA foi diluído com acréscimo de água ultrapura, para padronizar concentração do DNA em 10 ng/mL; contudo, devido às variações de pipetagem, as concentrações variaram de 10 a 29 ng/μL.
Os componentes para PCR com volume final de 25 mL foram: água ultrapura q.s.p. (Invitrogen Life TechnologiesTM, Brasil); 2,5 mL de tampão de PCR 10X (10 mM de Tris-HCl pH 8 e 50 mM de KCl (Invitrogen Life TechnologiesÒ, Carlsbad, CA, EUA); 4mM de MgCl2 (InvitrogenÒ); 0,25 mM de dNTPs (desoxiribonucleotídeo 5'- triophosphates – dATP, dCTP, dGTP e dTTP – GE Heathcare, Piscataway NJ, EUA); 15 pmol de cada oligonucleotídeo (PCO4/GH20 - InvitrogenÒ); 1U de Taq DNA polimerase (Invitrogen). Após a mistura, em outra sala de procedimentos e sob fluxo laminar, foram adicionados 5 mL do DNA de cada amostra. Controles positivo e negativo foram utilizados em todas as reações.
As reações foram conduzidas em um termociclador com a seguinte programação: desnaturação inicial a 95oC/10 minutos, seguida de 40 ciclos de desnaturação a 95oC/1 minuto, hibridização a 65oC/1 minuto e extensão a 72oC/2 minutos, seguidos de extensão final a 72oC/8 minutos. Os produtos de PCR para o gene β-globina (268 pares de base) foram analisados por eletroforese em gel de agarose a 2%, corados em brometo de etídio, visualizado sob luz ultravioleta e documentado com Sistema Kodak Digital Science1D®.
Resultados
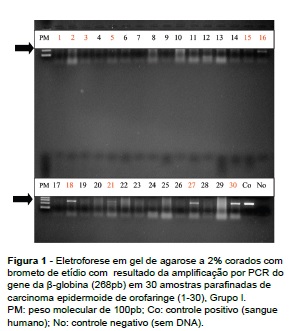
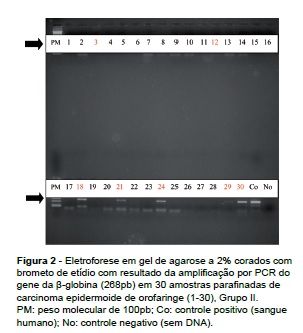
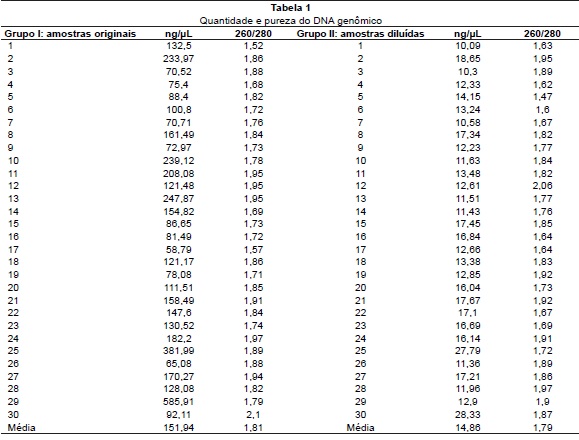
No Grupo I, 10 amostras de 30 (33,33%) foram positivas (amostras 1, 2, 3, 5, 15, 16, 18, 21, 27 e 30) para a amplificação do gene β-globina (Figura 1), sendo que a concentração das amostras variou de 58,79 a 585,91 ng/mL, com média de 151,94 ng/mL, e a razão 260/280 variou de 1,52 a 2,1 (Tabela 1). Cabe ressaltar que cada amostra foi quantificada três vezes e os valores supracitados representam a média. No Grupo II, 7 amostras de 30 (23,33%) foram positivas (3, 12, 18, 21, 24, 29 e 30) para a amplificação do gene β-globina (Figura 2), sendo que a concentração das amostras variou de 10,09 a 28,33 ng/mL, com média de 14,86 ng/mL, e a razão 260/280 variou de 1,47 a 2,06 (Tabela 1). Das 10 amostras positivas do Grupo I, quatro também foram positivas no Grupo II. Das sete amostras positivas no Grupo II, três foram negativas no Grupo I. A análise estatística revelou que não há diferença significativa entre os grupos (p=0,14).
Discussão
Neste trabalho, não houve diferença estatisticamente significativa nos resultados de positividade quanto à amplificação por PCR do gene da β-globina em amostras parafinadas. A literatura aponta uma grande diversidade na quantidade do DNA utilizada para a realização da PCR. Há relatos apenas do volume de DNA utilizado sem referência à sua concentração14,19, e apenas sobre a quantidade de DNA sem referência ao volume3,12,17, estudos em que o volume e a quantidade do DNA são descritos4,6,13,21,25 e, finalmente, estudos onde foi realizada a diluição pura e simples do DNA sem a padronização da concentração de DNA.
Após a diluição do DNA obtido a partir das amostras, a média da concentração das amostras foi de 14,86 ng/mL, considerando-se que utilizamos 5 mL de volume na PCR, e a média de DNA utilizada foi de 74,3 ng. Estes valores estão próximos aos utilizados por autores que obtiveram 55% de amostras amplificadas13, índice superior ao do presente trabalho, que foi de 23,33% de positividade para amplificação do gene β-globina. Vale lembrar que segundo An e Fleming1, quantidades menores que 50 ng de DNA em reações de PCR podem causar falhas na amplificação deste gene.
Considerando que a diluição do DNA frequentemente reduz o número de inibidores e contaminantes e ainda assim possui DNA suficiente para a amplificação em PCR24, era de se esperar uma melhora na taxa de amplificação, pois a média de concentração DNA do Grupo I foi de 151,94 ng/mL e do Grupo II de 14,86 ng/mL, ou seja, praticamente 10 vezes menor. Por outro lado, alguns autores consideram que um grande aumento na quantidade de DNA não influencia na taxa de amplificação, desde que use uma concentração de até 2000 ng de DNA por reação1.
A quantidade de material parafinado para iniciar a extração de DNA não parece ser essencial para o sucesso da PCR, pois existem bons resultados com cortes histológicos de 5, 10 ou 100 μm12. Vale ressaltar que a quantidade de tecido utilizada na etapa da extração do DNA foi padronizada em 25 mg, de acordo com as orientações do fabricante do sistema de extração de DNA QIAamp DNA minikit (Quiagen). Grandes quantidades de tecido podem conter grandes quantidades de inibidores da PCR12,16, desta forma uma quantidade maior que 25 mg poderia prejudicar a extração de DNA de boa qualidade. Um trabalho relata que a qualidade do tecido, neste caso representado pela celularidade, é que deve ser o fator determinante para avaliar a quantidade de tecido necessária para iniciar a extração1. No presente trabalho, os blocos de tecidos parafinados foram avaliados por meio de cortes histológicos previamente à coleta do material e foi confirmada a existência de neoplasia, que consiste em tecido extremamente celularizado, o que resulta em um bom material para realizar a extração do DNA.
Alguns autores consideraram que a detecção de fragmentos maiores do que 200 pares de base não é obtida com sucesso a partir de material parafinado1,20, porém outros autores referem ter conseguido ótimos resultados com fragmentos acima de 400 pb23. No presente trabalho, utilizou-se o gene β-globina em fragmento de PCR com 268 pares de bases e houve dificuldade de amplificação, porém em estudo anterior obteve-se 85,7% de amplificação pelo mesmo método25. Ainda segundo Cao et al. 4, a amplificação de um gene, levando-se em consideração seu tamanho, depende do método de extração utilizado. Fatores como a presença de substâncias inibidoras1,7 e a degradação do DNA pelas substâncias fixadoras dos tecidos, tais como o formol, podem ter influenciado a taxa de detecção do gene β-globina no presente estudo.
Outra tentativa de melhorar a eficiência de amplificação da PCR poderia ser a troca do método de extração e purificação do DNA, pois, nesta etapa, incluem-se passos que objetivam reduzir a concentração residual de proteínas e componentes da membrana que possam inibir a atividade da Taq polimerase18. Alguns autores relatam que o método fenol clorofórmio apresenta melhores resultados quando comparado ao sistema ora empregado 4,5.
Apesar de a análise de absorbância (260/280) das amostras serem compatíveis com percentuais encontrados na literatura 4, a quantidade de amostras positivas foi muito baixa. A diminuição da quantidade de DNA no ensaio visando a diminuir o excesso de substâncias inibidoras foi tentada. Isto é frequente na extração de DNA a partir de amostras de sangue, pois a diluição do DNA também diminui os íons Fe++ que são competidores dos íons Mg++, necessários à ação da DNA polimerase7,11.
Apesar de não ter sido estatisticamente significativo, o presente trabalho apontou a diminuição da taxa de amplificação positiva do gene estudado. O insucesso pode ter ocorrido em razão da degradação do DNA das amostras, assim como em outros trabalhos2,15.
No Grupo I, seis amostras positivas com DNA originalmente extraído não foram amplificadas após a diluição, demonstrando que a diluição não foi a melhor forma para aumentar a quantidade de amostras positivas amplificadas por PCR.
Por outro lado, cabe ressaltar que três amostras positivas do Grupo II não haviam sido amplificadas utilizando-se o DNA do Grupo I. Isso indica que a menor quantidade de DNA pode conter menos inibidores e favorecer a PCR, tornando a diluição uma opção na tentativa de aumentar o número de amostras positivas por PCR.
Conclusão
A diluição do DNA extraído de material parafinado não alterou estatisticamente a quantidade de amostras positivas por PCR para o gene β-globina, embora os resultados obtidos sugiram que esta seja uma das formas de aumentar a eficácia do método de amplificação por PCR.
Referências
1. An SF, Fleming KA. Removal of inhibitor(s) of the polymerase chain reaction form formalin fixed, paraffin wax embedded tissues. J Clin Pathol. 1991;44(11):924-7. [ Links ]
2. Barea JA, Pardini MIMC, Gushiken T. Extração de DNA de materiais de arquivo e fontes escassas para utilização em reação de polimerização em cadeia (PCR). Rev Bras Hematol Hemoter. 2004;26(4):278-81.
3. Camargo LL, Rivero ERC Nunes FD. Detecção de HHV-8 em sarcomas de Kaposi da mucosa bucal. RPG. 2005;12(2):174-8.
4. Cao W, Hashibe M, Rao JY, Morgenstern H, Zhang ZF. Comparison of methods for DNA extracted from paraffin-embedded tissues and bucal cells. Cancer Detect Prev. 2003;27(5):397-404.
5. Chan PK, Chan DP, To KF, Yu MY, Cheung JL, Cheng AF. Evaluation of extraction methods from paraffin wax embedded tissues for PCR amplification of human and viral DNA. J Clin Pathol. 2001;54(5):401-3.
6. Coura R, Prolla JC, Meurer L, Ashton-Prolla P. An alternative protocol for DNA extraction from formalin fixed and paraffin wax embedded tissue J Clin Pathol. 2005;58(8):894–5.
7. de Franchis R, Cross NC, Foulkes NS, Cox TM. A potent inhibitor of Taq polymerase copurifies with human genomic DNA. Nucleic Acids Res. 1988;16(21):10355.
8. Fernandes JV, Meissner RV, Fernandes TAAM, Rocha LRM, Cabral MC, Villa LL. Comparação de três protocolos de extração de DNA a partir de tecido fixado em formol e incluído em parafina. J Bras Patol Med Lab. 2004;40(3):141-6.
9. Goelz SE, Hamilton SR, Vogelstein B. Purification of DNA from formaldehyde-fixed and paraffin-embedded human tissue. Biochem Biophys Res Commun. 1985;130(1):118-26
10. Greer CE, Wheeler CM, Manos MM. Sample preparation and PCR amplification from paraffin-embedded tissues. PCR Methods Appl. 1994;3(6):113-22.
11. Gribben JG, Freedman A, Woo SD, Blake K, Shu RS, Freeman G, et al. All advanced stage non-Hodgkin's lymphomas with a polymerase chain reaction amplifiable breakpoint of bcl-2 rearrangement at evaluation and after treatment. Blood. 1991;78(12):3275-80.
12. Legrand B, Mazancourt P, Durigon M, Khalifat V, Crainic K. DNA genotyping of unbuffered formalin fixed paraffin embedded tissues. Forensic Sci Int. 2002;125(2-3):205-11.
13. Liborio TN, Etges A, Neves AC; Mesquita RA, Nunes FD. Evaluation of genomic DNA extracted from formalin-fixed, paraffin-embedded oral samples archives for the past 40-years. J Bras Patol Med Lab. 2005;41(6):405-10.
14. Lindel K, Beer KT, Laissue J, Greiner RH, Aebersold DM. Human papillomavirus positive squamous cell carcinoma of the oropharynx. A radiosensitive subgroup of head and neck carcinoma. Cancer. 2001;92(4):805-13.
15. Liu J, Johnson RM, Traweek ST. Rearrangement of the BCL-2 gene in follicular lymphoma. Detection by PCR in both fresh and fixed tissue samples. Diagn Mol Pathol. 1993;2(4): 241-7.
16. Lo YM, Mehal WZ, Fleming KA. In vitro amplification of hepatitis B virus sequences from liver tumour DNA and from paraffin wax embedded tissues using the polymerase chain reaction. J Clin Pathol. 1989;42(8):840-6.
17. Matizonkas-Antonio LF, de Mesquita RA, de Souza SC, Nunes FD. TP53 Mutations in Salivary Gland Neoplasms. Braz Dent J. 2005;16(2):162-6.
18. Merkelbach S, Gehlen J, Handt S, Füzesi L. Novel enzyme immunoassay and optimized DNA extraction for the detection of polymerase-chain-reaction-amplified viral DNA from paraffin-embedded tissue. Am J Pathol. 1997;150(5):1537-46.
19. Nemes JA, Deli L, Nemes Z, Márton IJ. Expression of p16INK4A, p53 and Rb proteins are independent from the presence of human papilomavirus genes in oral squamous cell carcinoma. Oral Surg Oral Med Oral Pathol Oral Radiol Endod. 2006;102(3):344-52.
20. Paabo S. Ancient DNA: extraction, characterization, molecular cloning and enzymatic amplification. Proc Natl Acad Sci USA. 1989;86(6):1939-43.
21. Santos MC, Saito CP, Line SR. Extraction of genomic DNA from paraffin-embedded tissue sections of human fetuses fixed and stored in formalin for long periods. Pathol Res Pract. 2008;204(9):633-6.
22. Schulz TF. Kaposi's sarcoma-associated herpesvirus (human herpesvirus 8): epidemiology and pathogenesis. J Antimicrob Chemother. 2000;45(T3Suppl):15-7.
23. Sepp R, Szabó I, Uda H, Sakamoto H. Rapid techniques for DNA extraction from routinely processed archival tissue for use in PCR. J Clin Pathol. 1994;47(3):318-23.
24. Shibata D. Extraction of DNA from paraffin-embedded tissue for analysis by polymerase chain reaction: new tricks from an old friend.Hum Pathol. 1994;25(6):561-3.
25. Simonato LE, Garcia JF, Nunes CM, Miyahara GI. Avaliação de dois métodos de extração de DNA de material parafinado para amplificação em PCR. J Bras Patol Med Lab. 2007;43(2):121-7.
Endereço para correspondência:
Glauco Issamu Miyahara
Rua José Bonifácio, 1193 – Vila Mendonça Araçatuba (SP), Brasil
CEP: 16015-050
e-mail: miyahara@foa.unesp.br
Recebido em: 28/08/09
Aceito em: 09/12/09