Serviços Personalizados
Artigo
Links relacionados
Compartilhar
Odontologia Clínico-Científica (Online)
versão On-line ISSN 1677-3888
Odontol. Clín.-Cient. (Online) vol.10 no.3 Recife Jul./Set. 2011
ARTIGO ORIGINAL / REVIEW ARTICLE
Análise e utilização de biomaterial confeccionado a partir das conchas de crassostrea gigas em defeito periodontal em ratos
Biomaterial's analysis and use, made of crassostrea gigas shells in rats' periondontal defects
Ulysses de AlmeidaI; João César ZielakII; Marcelo FilietazI; Allan Fernando GiovaniniII; Tatiana Miranda DeliberadorII; Lucienne Miranda UlbrichIII; Carla Castiglia GonzagaII
I Mestrado Profissional em Odontologia Clínica, Universidade Positivo
II Professor Doutor do Mestrado Profissional em Odontologia Clínica, Universidade Positivo
III Professora do Mestrado Profissional em Odontologia Clínica, Universidade Positivo
RESUMO
As conchas de ostras podem se apresentar como fonte promissora na confecção de biomaterial para enxertia óssea, uma vez que apresentam, na sua constituição principal, o cálcio. Este trabalho teve por objetivo avaliar os efeitos de um biomaterial obtido a partir da concha da Crassostrea gigas na sua aplicação, em defeitos periodontais de ratos. Análise das partículas por MEV revelou tamanhos variados e superfície microporosa e, por EDXRF, demonstrou uma constituição básica de CaO. Dois grupos de vinte ratos receberam defeito periodontal, preenchidos com coágulo sanguíneo ou com biomaterial teste. Os tempos de monitoramento foram de 1, 3, 6 e 8 semanas. A análise histológica do biomaterial teste revelou: um processo inflamatório granulomatoso crônico; mais edema do que o controle; inicialmente, o aparecimento de um tecido osteoide mais fibroso, que resultou em um reparo ósseo em camadas finas, que, além de aspecto fibroplásico no ligamento periodontal, em estágio mais avançado, transformou-se em anquilose. Pode-se concluir que a aplicação do biomaterial no defeito periodontal deste trabalho não foi favorável.
Descritores: Crassostrea; Defeito periodontal; Doenças Periodontais; Transplante Ósseo; Materiais Biocompatíveis.
ABSTRACT
Oyster shells may be presented as a potential source for the production of a bone graft biomaterial, once they are mainly constituted by calcium. The aim of this study was to evaluate the effects of a biomaterial based on Crassostrea gigas shell in the application of periodontal defects in rats.MEV analysis of the particles showed a variety of sizes and microporous surface, while EDXRF analysis demonstrated calcium oxide as the main component. Two groups of 20 WISTAR rats received periodontal defects filled with either blood clot or the test biomaterial. Monitoring periods were 1, 3, 6 and 8 weeks. Histological analysis revealed a chronic granulomatous process; more edema than control; an initial fibrous osteoid tissue; a thin layered bone repair; a fibroplasic aspect of the periodontal ligament; and in an advanced stage, ankylosis. It can be concluded that the application of the biomaterial in the periodontal defect of this study was unfavorable.
Keywords: Crassostrea; Periodontal defect; Bone substitute; Periodontal Dislases; Bone Transplantation; Biocomplative Materials.
INTRODUÇÃO
O conhecimento histofisológico do osso e a intenção de reproduzir tal tecido são de fundamental importância nas especialidades de Estomatologia, Cirurgia e Traumatologia Buco-Maxilo-Facial, Periodontia e Implantodontia.
Sabe-se que o sistema de suporte ósseo é fundamental para a manutenção dos elementos dentários, vice-versa. A doença periodontal, por exemplo, pode levar à perda óssea, que, por sua vez, leva à perda dentária, afetando o indivíduo estética e funcionalmente1. Assim, por causa da perda precoce de dentes, ligada ao processo fisiológico de reabsorção óssea, além da pneumatização dos seios maxilares, muitos pacientes necessitam de uma reconstrução óssea prévia. A perda óssea é um problema para a função mastigatória e gera um grande impacto social, especialmente em pessoas com mais idade2.
A reposição óssea pode ser realizada com uso de osso autógeno, que é considerado o material mais eficiente para tal procedimento3. Outra opção é o uso de biomateriais, entre eles os xenogênicos (de outra espécie), que podem apresentar benefícios, como a semelhança com o osso humano e a utilização de bens renováveis pela própria natureza. Um exemplo clássico é o uso do osso bovino como biomaterial de enxerto4.
Dentre os xenogênicos, também existem fontes alternativas usadas na produção de biomateriais, tais como a casca de ovos de avestruz5 e as conchas marinhas6. Conchas de ostras podem se apresentar como fonte promissora na confecção de biomaterial para enxertia óssea, uma vez que apresentam como constituinte principal a calcita, um cristal à base de carbonato de cálcio, e, além disso, demonstram, em sua parte orgânica, moléculas praticamente idênticas às encontradas em humanos: BMP-2 (bone morphogenetic protein)7.
As BMPs foram bem descritas em um estudo clássico de 1967, no qual Urist et al.8 demonstraram pesquisas com substitutos ósseos, visando encontrar um material ideal para reconstruir o osso humano com base no princípio de que as BMPs contribuem para a diferenciação celular.
Assim, visando à diminuição de custos, o aproveitamento de fontes renováveis para a produção de biomateriais e buscando fornecer informações histológicas no que se refere à viabilidade de eventual aplicação clínica futura em humanos, o objetivo deste estudo foi o de avaliar os efeitos de um biomaterial obtido a partir da concha da Crassostrea gigas na sua aplicação em defeitos periodontais de ratos.
MATERIAL E MÉTODOS
Todos os procedimentos foram aprovados pelo Comitê de Ética no Uso de Animais da Universidade Positivo (148/2008).
Foram utilizadas conchas de ostras, Crassostrea gigas, oriundas do descarte da indústria alimentícia (Bombinhas, SC, Brasil). As conchas foram lavadas e escovadas em água corrente, e os resíduos remanescentes da limpeza foram removidos por máquina para polimento de prótese (disco de óxido de alumínio, 20.000 rpm, Politrix, Nevone, São Paulo, SP, Brasil). Após a limpeza, as conchas foram moídas em pilão manual (Kopp, Curitiba, PR, Brasil), e as partículas produzidas foram autoclavadas (Vitale Plus 12, Cristófoli, Campo Mourão, PR, Brasil).
ANÁLISE QUÍMICA E MICROSCOPIA DAS PARTÍCULAS
A EDXRF (Espectrometria de fluorescência de raios-X por energia dispersiva) foi realizada de acordo com metodologia previamente descrita9,10. Uma pequena quantidade das partículas foi colocada em suporte, metalizada (SCD 030, Balzers Union, Alemanha) e observada em microscópio eletrônico de varredura (MEV, JSM6360-Lv, Jeol, Tóquio, Japão).
PROCEDIMENTOS CIRÚRGICOS
Foram utilizados 40 ratos (Rattus norvergicus), machos, de seis meses de idade, com peso entre 350 e 450 gramas, os quais foram divididos em dois grupos: grupo-controle (C) e grupo experimental de teste (T), subdivididos em cinco animais para cada subgrupo. Foram submetidos à sedação por halotano (Bayer, Alemanha) e anestesiados com quetamina (40 mg/kg, Bayer, Alemanha) e xilazina (5 mg/kg, Bayer, Alemanha), via intraperitoneal. Em sequência, o ato cirúrgico se constituiu inicialmente de uma incisão linear (aproximadamente 8 mm) na porção direita da mandíbula, na região vestibular e anterior ao forame mentual, com lâmina de bisturi 15 (BD, São Paulo, SP, Brasil), sem romper o colarinho cervical. Após afastamento da gengiva e do periósteo, fez-se a criação do defeito ósseo por ação de broca esférica multilaminada (carbide) de 3mm de diâmetro (Antilope, Suíça), adaptada em aparelho portátil de baixa rotação (Dentec-405N, Rio de Janeiro, RJ, Brasil), de acordo com protocolo cirúrgico pré-estabelecido11.
No grupo C, o defeito foi preenchido apenas com coágulo, e no grupo T, com o biomaterial experimental. Os animais receberam sutura com dois pontos simples, usando fio de nylon 5.0 (Procare, Lamedid, Barueri, São Paulo, Brasil), e, ao término da cirurgia, receberam uma dose de morfina (1mL, Bayer, Alemanha). A eutanásia dos animais foi realizada em câmara de gás de CO2, conforme os tempos de monitoramento de 1, 3, 6 e 8 semanas. Todos os procedimentos cirúrgicos foram realizados pelo mesmo operador.
PROCEDIMENTOS HISTOLÓGICOS
As hemimandíbulas com os defeitos foram coletadas e fixadas em formol neutro a 10% (Sulana, Maringá, Paraná, Brasil), lavadas e descalcificadas em solução de ácido fórmico a 10% (Sigma, Diadema, São Paulo, Brasil). As peças foram processadas e incluídas em parafina. Foram feitos cortes seriados de 5 μm de espessura, no sentido mésio-distal, e a coloração por HE. Para análise histológica, as imagens foram coletadas por microscópio (021/3 Quimis, Diadema, SP, Brasil) e câmera acoplada (SDC-310, Samsung, Coreia). Os aumentos utilizados foram de 40, 100 e 400 ×, nos quais se analisaram os parâmetros: fechamento do defeito, edema, reparo ósseo e reparo do ligamento periodontal.
RESULTADOS
Análise por mev
O aspecto ultraestrutural demonstrou a produção de partículas de tamanhos aproximados de 20 a 700 μm (Figuras 1A e 1B). Em aumentos maiores de 1500 a 10000 ×, pode-se observar a irregularidade da superfície do biomaterial, visto que as partículas aparentam ser formadas pela união de cristais menores (Figuras 1C e 1D).

Análise por edxrf
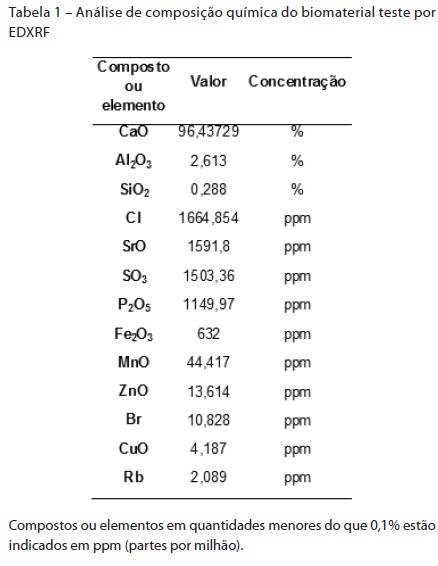
O óxido de cálcio (CaO) predominou, com aproximados 96% da composição do biomaterial. (Tabela 1)
Observações clínicas
O biomaterial teste demonstrou características favoráveis de manipulação durante a aplicação cirúrgica, mantendo-se aglutinado e com grande estabilidade em contato com tecidos vivos. Após os procedimentos cirúrgicos, os animais se alimentaram normalmente, apresentaram aspectos clínicos normais, com comportamento similar, e resposta inflamatória cicatricial.
Análise histológica
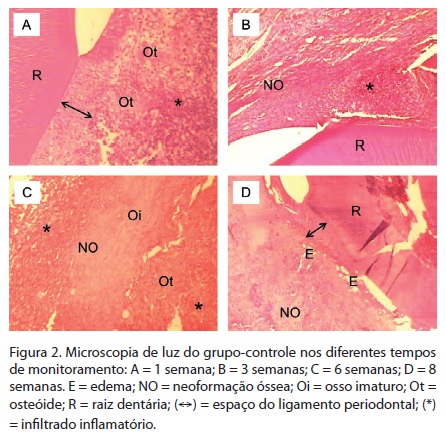
No grupo controle de 1 semana, foram identificadas áreas com formação de tecido osteoide no meio do tecido de granulação (focal, apresentando processo inflamatório crônico) e áreas de neoformação de fibras colágenas, dispostas perpendicularmente ao tecido cementário, mimetizando ligamento periodontal, embora, em nenhum dos espécimes analisados, tenha se observado fechamento ósseo do defeito (Figura 2A).
No grupo-controle de 3 semanas, pode-se constatar áreas com proliferação óssea a partir das margens do defeito, e um tecido de granulação localizado focalmente, caracterizado pelo processo inflamatório crônico disperso. (Figura 2B) No grupo controle de 6 semanas, foi constatado o fechamento do defeito cirúrgico em todos os espécimes, a partir da presença de osso neoformado maduro e imaturo coaptando as bordas, sendo evidente a presença de um tecido de granulação composto por fibroplasia e processo inflamatório crônico, predominantemente linfo-plasmocitário, nas regiões ligamentar e submucosa (Figura 2C). Já no grupo controle de 8 semanas observou-se ainda melhor coaptação das margens do defeito nos cortes histológicos, o que refletiu no fechamento completo do defeito. Além disso, foi observada a presença de tecido de granulação restrita ao centro do defeito e predominância de aspectos de normalidade das regiões ligamentar e submucosa. (1A)
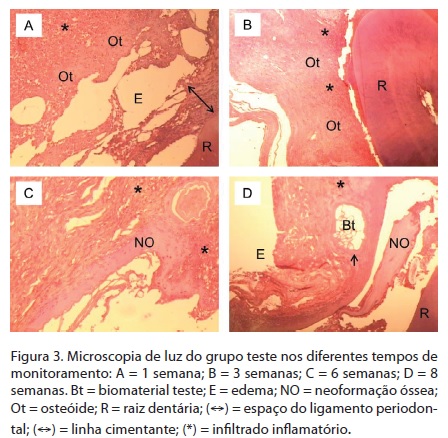
No grupo teste de 1 semana, identificou-se a formação de tecido mineral semelhante ao tecido ósseo, em permeio a intenso processo inflamatório crônico e agudo. Em nenhum dos espécimes analisados, foi observado o fechamento ósseo do defeito (Figura 3A). No grupo teste de 3 semanas, constatou-se a formação de áreas de tecido osteoide dispostas em mosaico, circundadas por área de intensa fibroplasia. Houve processo inflamatório crônico inespecífico, sem fechamento ósseo do defeito. (Figura 3B)
No grupo teste de 6 semanas foi observada a formação de uma fina ponte óssea sobre a área do defeito, com um processo inflamatório crônico exibindo edema intenso em região ligamentar. A região submucosa estava em remodelamento. Houve fechamento parcial dos defeitos em todo grupo (Figura 3C). No grupo teste de 8 semanas observou-se a coaptação de bordas formada por tecido mineral fino e irregular, calcificação de matriz na região ligamentar semelhante a uma anquilose, além da presença de tecido inflamatório crônico, e o fechamento dos defeitos com tecido mineral irregular fino em todas as amostras. (Figura 3D)
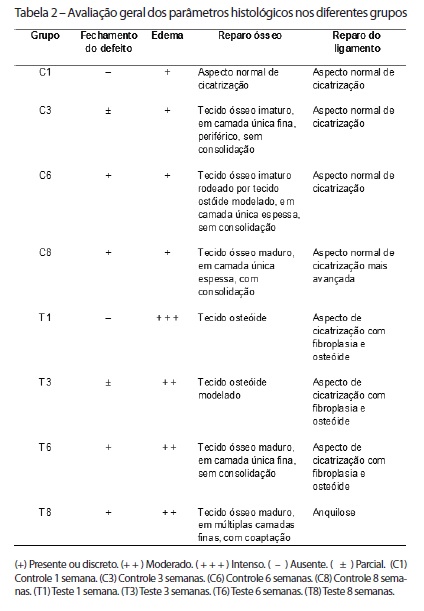
A Tabela 2 mostra a comparação dos resultados entre os grupos em estudo.
DISCUSSÃO
A ideia de se usar um biomaterial de descarte, como é o caso da concha deste trabalho, esteve contemporaneamente afinada com a filosofia da sustentabilidade, algo essencial para os dias de hoje. A análise química inicial do biomaterial teste confirmou a hipótese de que o principal constituinte seria o cálcio, como observado na Tabela 1, em algum tipo de óxido.
Acredita-se que os efeitos das BMP-2 na morfogênese e formação óssea ocorram a partir da união de dois tipos de receptores kinase serina/treonina (receptores tipo I e II). Ambos são essenciais para a transdução do sinal da BMP12,13. Estudos recentes revelam que moléculas semelhantes às sinalizadoras (BMP-2) para a formação óssea em humanos são encontradas em conchas Crassotrea gigas14. Tais moléculas podem estar presentes na camada nacre da concha, como acontece na espécie Pinctada fucata7. Isso também corrobora para justificar a escolha da fonte de matéria-prima para o desenvolvimento do biomaterial teste aqui apresentado.
Com relação aos testes in vivo, como em muitos outros estudos experimentais, o rato foi usado devido às vantagens em termos de facilidade de aquisição, manutenção e manipulação cirúrgica15. Este modelo específico apresenta uma similaridade com as situações clínicas de enxerto ósseo, devido ao defeito ser na boca do animal com acesso intrabucal. Assim, obteve-se um comportamento clínico mais realístico, pois o animal salivou normalmente sobre a região, ingeriu a alimentação e estimulou a região com a língua – o local esteve submetido a cargas constantes, como o que acontece normalmente na boca de um indivíduo. No entanto, o defeito não é caracterizado como crítico, sendo que seu diâmetro máximo foi de 3 mm, enquanto estudos relatam defeitos críticos com diâmetros de 5mm para o rato16.
Clinicamente, o material se comportou de maneira aceitável durante a sua manipulação, sendo facilmente incorporado à região do defeito, por característica de hidrofilia, o que permitiu sua aglutinação com o sangue. Também não houve sinais de abscessos ou infecção.
No presente estudo, a respeito de reparo ósseo, observou- se que durante a fase osteoide, tanto no grupo- controle (Figura 2C) quanto no grupo teste (Figura 3C), houve regiões de deposição de fibras de forma ordenada semelhante a um tecido modelado. Durante a fase de maturação, o aspecto das regiões com o osso maduro se apresentou normal, principalmente nos cortes de espécimes do grupo- controle (Figuras 2B, 2C e 2D). Nos cortes histológicos do grupo teste, o osso maduro formado encontrado foi mais fino, em camadas múltiplas (com tendência à baixa adesão entres as camadas, fato que se observa com o aparecimento de espaços entre elas) (Figura 3D), e com número menor de osteócitos (Figuras 3C e 3D) do que o osso maduro observado em cortes do grupo controle. Em relação à matriz orgânica, durante a fase de osteoide, sabe-se que modificações diferenciais nas orientações das deposições de colágeno e mineral, durante a neoformação óssea, podem acontecer como adaptações ultraestruturais da matriz, com a finalidade de se obter resistência ótima, ou acomodação à micro fraturas, em regiões suscetíveis às tensões mecânicas17,18.
Além disso, pode-se perceber que o tecido osteoide no grupo teste, em determinadas regiões (Figura 3A), apresentou um aspecto mais denso, provavelmente mais fibroso, do que o controle (Figura 2A). Este mesmo aspecto mais denso se refletiu no reparo do ligamento das amostras do grupo teste (Figura 3). Um outro achado importante observado no último período de monitoramento (8 semanas) foi o fato de que a fibroplasia, com aspecto osteoide da região do ligamento, caracterizou-se como uma anquilose, ou seja, culminou com a mineralização do ligamento periodontal. Em condições normais, o ligamento periodontal se apresenta como um tecido conjuntivo , altamente organizado com feixes de fibras, um conteúdo fluido e um sistema vascular que são características importantes para o desempenho de suas funções19. Em relação à união das partículas do biomaterial teste com o osso, pode-se observar (Figura 3D), em 8 semanas, que estavam aderidas ao tecido neoformado ao seu redor por meio de uma linha cimentante. De acordo com Davies20, esta linha cimentante representa não apenas uma união química do osso com a superfície do biomaterial, mas uma interdigitação micromecânica, possivelmente de proteínas não colagenosas, sinal favorável à migração de osteoclastos, ou seja, ao remodelamento. Este achado pode indicar a possibilidade de incorporação do biomaterial ao osso. Nas semanas iniciais (1 a 3), a presença do biomaterial teste nos cortes histológicos não foi evidente, provavelmente devido a uma maior intensidade do edema ao redor das partículas, o que pode ter promovido o deslocamento destas durante o processamento histológico. Neste mesmo modelo e período, em trabalho descrito anteriormente21, observa-se um infiltrado inflamatório crônico e agudo, além da presença de células gigantes e vascularização aumentadas em relação ao grupo controle - características não evidentes no presente trabalho.
Outro resultado interessante foi o fato de que, em cortes do grupo teste, o tecido ósseo neoformado na região do enxerto produziu um reparo ósseo em camadas finas que visivelmente se dissociaram (Figuras 3B, 3C e 3D). Nesse ponto, talvez por ação da linha cimentante presente em camadas ósseas, o remodelamento poderia ter sido estimulado de forma mais rápida do que o que aconteceu com o grupo controle, que, por sua vez, demonstrou uma tendência a neoformar uma camada única e mais espessa (Figura 2C). O fato de se observarem células (fibroblastos) em permeio a material extracelular, dentro de partículas do biomaterial teste comprova que este possui microporosidades compatíveis com o crescimento celular. É demonstrado que o aumento na área da superfície de materiais à base de cálcio, como é o caso dos biomateriais de enxerto ósseo, pode favorecer a adsorção de proteínas do meio intersticial22, e por consequência, atrair as células importantes para a formação do tecido. Segundo a análise por MEV do biomaterial teste, pode-se observar que as partículas apresentaram grande porosidade e uma superfície bastante irregular. (Figura 1)
Pelas características de incorporação e união da matriz óssea neoformada com as partículas, o biomaterial teste pareceu ter mecanismo de ação semelhante ao do biovidro. Uma vez que o biomaterial teste apresentou proliferação celular dentro de microporosidades (Figura 3D), pode-se discutir um perfil de aplicação para esse biomaterial teste: arcabouço.
Para se elaborar um arcabouço, vários fatores devem ser considerados. Preferencialmente, o arcabouço deve degradar de acordo com a nova formação tecidual, deve ser biocompatível, e seus produtos de degradação também devem ser biocompatíveis. Uma vez implantado, deve possuir propriedades mecânicas necessárias para oferecer apoio estrutural temporariamente, até que a formação de um novo tecido ocorra. Além disso, o arcabouço deve possuir características morfológicas importantes, como a alta porosidade e disponibilidade de oferecer uma passagem viável para a transmissão de nutrientes e crescimento tecidual interno, além de propiciar a angiogênese. Para obter tais características, os arcabouços são frequentemente desenhados para imitar a estrutura de uma matriz extracelular natural23. Hoje os arcabouços são biomateriais de desenvolvimento desafiador para a atual engenharia de tecidos24.
Sugere-se que o biomaterial teste do presente trabalho deva ser mais aprofundadamente avaliado. Para aplicações clínicas em região periodontal, os resultados aqui apresentados não se revelaram satisfatórios devido à formação de anquilose. Contudo, em defeitos ósseos que não envolvam a superfície radicular, o biomaterial teste pode apresentar um melhor desempenho.
CONCLUSÃO
De acordo com as informações descritas no presente trabalho, a utilização do biomaterial confeccionado a partir da concha da Crassostrea gigas promoveu inicialmente o aparecimento de um tecido osteoide mais fibroso que resultou em um reparo ósseo em camadas finas, além de aspecto fibroplásico no ligamento periodontal que, em estágio mais avançado, transformou-se em anquilose. Assim, pode-se concluir que a aplicação do biomaterial no defeito periodontal deste trabalho não foi favorável.
REFERÊNCIAS
1. Bodic F, Hamel L, Lerouxel E, Basle MF, Chappard D. Bone loss and teeth. Joint Bone Spine. 2005 May;72(3):215-21. [ Links ]
2. Turkyilmaz I, Patel NS, McGlumphy EA. Oral rehabilitation of a severely resorbed edentulous maxilla with screwed-retained hybrid denture using cresco system: a case report. Eur J Dent. 2008 July;2(3):220-3.
3. Shegarfi H, Reikeras O. Review article: bone transplantation and immune response. J Orthop Surg (Hong Kong). 2009 Aug;17(2):206-11.
4. Stavropoulos A, Karring T. Guided tissue regeneration combined with a deproteinized bovine bone mineral (Bio-Oss) in the treatment of intrabony periodontal defects: 6-year results from a randomized-controlled clinical trial. J Clin Periodontol. 2010 Feb;37(2):200-10.
5. Dupoirieux L. Ostrich eggshell as a bone substitute: a preliminary report of its biological behaviour in animals--a possibility in facial reconstructive surgery. Br J Oral Maxillofac Surg. 1999 Dec;37(6):467-71.
6. Lamghari M, Berland S, Laurent A, Huet H, Lopez E. Bone reactions to nacre injected percutaneously into the vertebrae of sheep. Biomaterials. 2001 Mar;22(6):555-62.
7. Miyashita T, Hanashita T, Toriyama M, Takagi R, Akashika T, Higashikubo N. Gene cloning and biochemical characterization of the BMP-2 of Pinctada fucata. Biosci Biotechnol Biochem. 2008 Jan;72(1):37-47.
8. Urist MR, Silverman BF, Buring K, Dubuc FL, Rosenberg JM. The bone induction principle. Clin Orthop Relat Res. 1967 July/Aug;53:243-83.
9. Avigo D, Jr., Godoi AF, Janissek PR, Makarovska Y, Krata A, Potgieter-Vermaak S, et al. Particulate matter analysis at elementary schools in Curitiba, Brazil. Anal Bioanal Chem. 2008 June; 391(4):1459-68.
10. Vazquez C, Custo G, Dawidowski L, Gomez D, Villegas M, Ortiz M, et al. Elucidating a particulate matter deposition episode by combining scanning electron microscopy and X-ray fluorescence spectrometry. Anal Sci. 2005 July; 21(7):763-7.
11. Zielak JC, Mathias AL, Almeida S, Giovanini AF. Oral Bone Grafting in a Rat Model and the use of Scanning Eletron Microscopy for Tissue Morfology Evaluation. Scandinavian Journal of Laboratory Animal Science. 2007; (34):201-10.
12. Rosenzweig BL, Imamura T, Okadome T, Cox GN, Yamashita H, ten Dijke P, et al. Cloning and characterization of a human type II receptor for bone morphogenetic proteins. Proc Natl Acad Sci U S A. 1995 Aug 15;92(17):7632-6.
13. Wan M, Cao X. BMP signaling in skeletal development. Biochem Biophys Res Commun. 2005 Mar 18;328(3):651-7.
14. Herpin A, Lelong C, Becker T, Rosa F, Favrel P, Cunningham C. Structural and functional evidence for a singular repertoire of BMP receptor signal transducing proteins in the lophotrochozoan Crassostrea gigas suggests a shared ancestral BMP/ activin pathway. Febs J. 2005 Jul;272(13):3424-40.
15. Aaron RK, Wang S, Ciombor DM. Upregulation of basal TGFbeta1 levels by EMF coincident with chondrogenesis-implications for skeletal repair and tissue engineering. J Orthop Res. 2002 Mar;20(2):233-40.
16. Arosarena OA, Falk A, Malmgren L, Bookman L, Allen MJ, Schoonmaker J, et al. Defect repair in the rat mandible with bone morphogenic proteins and marrow cells. Arch Facial Plast Surg. 2003 Jan-Feb;5(1):103-8.
17. Noble BS, Reeve J. Osteocyte function, osteocyte death and bone fracture resistance. Mol Cell Endocrinol. 2000 Jan 25;159(1-2):7-13.
18. Skedros JG, Sorenson SM, Takano Y, Turner CH. Dissociation of mineral and collagen orientations may differentially adapt compact bone for regional loading environments: results from acoustic velocity measurements in deer calcanei. Bone. 2006 July; 39(1):143-51.
19. Natali AN, Pavan PG, Scarpa C. Numerical analysis of tooth mobility: formulation of a non-linear constitutive law for the periodontal ligament. Dent Mater. 2004 Sep;20(7):623-9.
20. Davies JE. Bone bonding at natural and biomaterial surfaces. Biomaterials. 2007 Dec;28(34):5058-67.
21. Zielak JC, Lopes DK, Giovanini AF, Filho FB, Mathias A. Histological evaluation of experimental bonegrafiting in vivo of lyophilized bovine bone. Rev Sul Bras Odont. 2007;4(1):22-8.
22. Zhu XD, Zhang HJ, Fan HS, Li W, Zhang XD. Effect of phase composition and microstructure of calcium phosphate ceramic particles on protein adsorption. Acta Biomater. 2010 Apr;6(4):1536-41.
23. Ma PX, Zhang R. Synthetic nano-scale fibrous extracellular matrix. J Biomed Mater Res. 1999 July; 46(1):60-72.
24. Smith IO, Liu XH, Smith LA, Ma PX. Nanostructured polymer scaffolds for tissue engineering and regenerative medicine. Wiley Interdiscip Rev Nanomed Nanobiotechnol. 2009 Mar/Apr;1(2):226-36.
 Endereço para correspondência:
Endereço para correspondência:
João César Zielak
R. Professor Pedro Viriato Parigot de Souza, 5300
Campo Comprido – Curitiba PR/Brasil
CEP: 81280-330
E-mail: jzielak2@gmail.com
Recebido para publicação: 11/04/11
Aceito para publicação: 19/04/11