Serviços Personalizados
Artigo
Links relacionados
Compartilhar
RGO.Revista Gaúcha de Odontologia (Online)
versão On-line ISSN 1981-8637
RGO, Rev. gaúch. odontol. (Online) vol.59 no.1 Porto Alegre Jan./Mar. 2011
ORIGINAL ORIGINAL
Análise da força de tração necessária para a remoção de cimento resinoso fixado em raízes preparadas com diferentes substâncias químicas
Analysis of the force required to remove resin cement from roots prepared with different chemicals
Gabriel Rocha CamposI; Rielson José Alves CardosoI; Marcelo Cavenaghi Pereira da SilvaII,*
IFaculdade São Leopoldo Mandic, Curso de Odontologia, Programa de Pós-Graduação em Endodontia. Rua José Rocha Junqueira, 13, Swift, 13045-755, Campinas, SP, Brasil
IIUniversidade Federal de São Paulo, Departamento de Morfologia e Genética. São Paulo, SP, Brasil
RESUMO
OBJETIVO: Avaliar in vitro, a influência das substâncias químicas utilizadas durante o preparo endodôntico na força de tração do cimento resinoso Rely-X (3M, Sumaré, Brasil) na dentina radicular bovina.
MÉTODOS: Utilizou-se 72 dentes bovinos que tiveram suas coroas seccionadas e raízes padronizadas. A seguir, os espécimes foram incluídos em blocos de resina e receberam tratamento químico por 10 minutos com hipoclorito de sódio nas concentrações de 0,5%, 1%, 2,5%, 5,25% ou gel de clorexidina a 2%, além do grupo-controle que recebeu água destilada. Em seguida os espécimes foram imersos em solução de EDTA a 17% por 3 minutos. Dois espécimes de cada grupo foram submetidos à microscopia eletrônica de varredura para avaliação da superfície. Os espécimes para o ensaio de teste de tração receberam condicionamento com ácido fosfórico a 37% por 15 segundos, sistema adesivo Single-Bond (3M, Sumaré, Brasil) e sobre este aplicado o cimento resinoso Rely-X (3M, Sumaré, Brasil).
RESULTADOS: Os resultados em Kgf foram: GClorex (2,26); GNaOCl-0,5% (7,92); GNaOCl-1% (9,70); GNaOCl-2,5% (9,05); GNaOCl-5,25% (8,91); GA (0,61).
CONCLUSÃO: O hipoclorito de sódio nas concentrações testadas aumentou a força de adesão do cimento resinoso na dentina de forma significativa frente água destilada e gel de clorexidina a 2%. A observação na microscopia eletrônica de varredura mostrou que a estrutura de dentina radicular que fora tratada com hipoclorito de sódio apresentava túbulos dentinários com diâmetros aumentados, menor quantidade de dentina intertubular, além de áreas de depressões, diferentemente dos grupos-controle e gel de clorexidina a 2%.
Termos de indexação: Cimentos de resina. Dentina. Endodontia.
ABSTRACT
OBJECTIVE: This study assessed in vitro how the chemicals used in the preparation of root canals affected the force required to remove the resin cement Rely-X (3M, Sumaré, Brazil) from bovine root dentin.
METHODS: The crowns of 72 bovine teeth were sectioned and the roots were standardized. The specimens were then placed in resin blocks and treated for 10 minutes with sodium hypochlorite at 0.5%, 1%, 2.5% or 5.25% or chlorhexidine gel at 2%. The control group was treated with distilled water. Next, the specimens were soaked in 17% EDTA for 3 minutes. The surfaces of two specimens from each group were assessed by electron scanning microscopy. The tested specimens were then treated with 37% phosphoric acid for 15 minutes, adhesive system Single-Bond (3M, Sumaré, Brazil) and the resin cement Rely-X (3M, Sumaré, Brazil) was applied over it.
RESULTS: The results in Kgf were: GChlorhex (2.26); GNaOCl-0.5% (7.92); GNaOCl-1% (9.70); GNaOCl-2.5% (9.05); GNaOCl-5.25% (8.91); GA (0.61).
CONCLUSION: Sodium hypochlorite in the tested concentrations increased the adhesion of the resin cement to the dentin significantly when compared with water and 2% chlorhexidine. Electron scanning microscopy showed that the structure of the root dentin treated with sodium hypochlorite presented widened dentinal tubules, less intertubular dentin and depression areas, all of which were not observed in the roots treated with water and 2% chlorhexidine gel.
Indexing terms: Resin cements. Dentin. Endodontics.
INTRODUÇÃO
A restauração final para os dentes tratados endodonticamente necessita de adequado procedimento para a conclusão do tratamento. Neste sentido, alguns fatores podem in-fluenciar como a atuação das substâncias químicas utilizadas durante o preparo dos sistemas de canais radiculares. O hipoclorito de sódio consagra-se como a solução irrigadora mais estudada e utilizada no preparo dos sistemas de canais radiculares, devido às características físico-químicas que apresentam, dentre elas, a de dissolução de tecido orgânico. A remoção da smear layer deve ser realizada por substâncias que removam a matéria inorgânica. Dentre elas, destacam-se as soluções quelantes que combinadas com o hipoclorito de sódio, produzem a limpeza da superfície e removem a smear layer. Assim, os túbulos dentinários ficam mais largos e permitem que os materiais obturadores e restauradores penetrem nesses canalículos.
A solução de clorexidina tem sido estudada como auxiliar do preparo endodôntico e apresenta resultados satisfatórios quanto as propriedades antimicrobianas, porém não apresenta características em relação à dissolução de matéria orgânica. As substâncias químicas, utilizadas durante o preparo biomecânico permanecem em contato com a dentina por períodos prolongados de tempo, provocando alterações na dentina que podem influenciar no sucesso da restauração final.
Nesse sentido a utilização de cimentos à base de resina para fixação de próteses coronárias e retentores intra-radiculares pode estar comprometida. O objetivo deste estudo foi avaliar in vitro a força necessária para tração do cimento resinoso Rely-XTM(3M, Sumaré, Brasil) e sistema adesivo Single BondTM (3M, Sumaré, Brasil) fixado na dentina radicular, após o preparo químico com hipoclorito de sódio nas concentrações de 0,5%, 1%, 2,5%, 5,25% e clorexidina em gel a 2%.
MÉTODOS
Preparo e embutimento das raízes
Para a realização deste estudo, foram utilizados 72 incisivos inferiores de bovinos. A seguir os dentes tiveram a coroa seccionada na porção cervical e, em seguida, seccionados longitudinalmente no sentido mésio-distal, sendo que o comprimento de cada espécime foi padronizado em 10mm, tomando-se como referência para mensuração a linha esmalte-cemento do dente.
Inclusão dos espécimes em resina
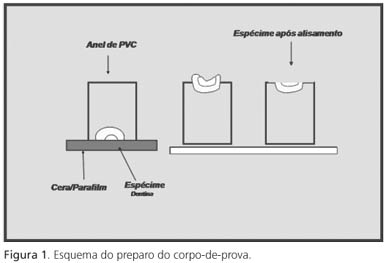
Para a inclusão dos espécimes, foram realizadas, transversalmente, retenções no cemento para uma maior fixação dos mesmos no bloco de resina. Foram então colocados sobre uma lâmina de cera número 7 envolta por uma película de Parafilm® (Aldrich, Milwaukee, EUA) com a face da dentina voltada para baixo. Em seguida, colocou-se, ao redor de cada espécime, um anel de PVC de diâmetro de três quartos de polegada por 20mm de altura, e foi vertida resina de Poliestireno no interior do anel de PVC até o seu total preenchimento.
Os espécimes preparados foram ainda submetidos a aplainamento, quando se utilizou uma politriz refrigerada e uma sequência de lixas de granulação de 400 e 600. Para a remoção do smear layer formado durante o preparo com as lixas, os dentes foram imersos em solução de EDTA 17% por 3 minutos1 (Figura 1).
Divisão dos grupos
Os espécimes foram divididos, aleatoriamente, em seis grupos com doze elementos para receber as seguintes soluções químicas:
Grupo 1: 10ml de digluconato de clorexidina gel a 2% (Endogel Endosupport, Itapetininga, Brasil) + 100ml água destilada;
Grupo 2: 100ml hipoclorito de sódio a 0,5%;
Grupo 3: 100 ml hipoclorito de sódio a 1%;
Grupo 4: 100 ml hipoclorito de sódio a 2,5%;
Grupo 5: 100ml hipoclorito de sódio a 5,25%;
Grupo 6: 100ml água destilada.
Preparo químico dos espécimes
Após a divisão dos grupos, estes foram colocados em recipientes plásticos de maior altura que os blocos com as raízes.
Em seguida, colocaram-se as soluções irrigadoras dos grupos de 2 a 6 até total preenchimento do recipiente plástico. As soluções foram renovadas a cada 1 minuto durante o período de 10 minutos.
Para o grupo 1 (gel de clorexidina), foi realizado aplicação com seringa descartável 1ml de gel de clorexidina sobre toda a superfície do espécime. Após 1 minuto, o espécime era lavado com água destilada e, novamente, repetia-se o tratamento pelo período total de 10 minutos.
Logo após, todos os grupos receberam secagem com papel absorvente e foram imersos em solução de EDTA a 17% pelo tempo de 3 minutos, sendo a solução utilizada renovada a cada minuto. Passado esse período, os espécimes foram lavados com água destilada para a remoção total do EDTA a 17%.
Preparo das amostras para microscopia eletrônica de varredura
Após o preparo químico, dois espécimes de cada grupo foram selecionados para a microscopia eletrônica de varredura. Primeiramente, os espécimes foram desidratados em série crescente de etanóis, em seguida, as peças foram metalizadas com ouro e examinadas em um microscópio eletrônico de varredura.
Inserção do cimento resinoso
Para inserção do cimento resinoso nos espécimes foi utilizado o sistema adesivo Single BondTM(3M, Sumaré, Brasil). O cimento de fixação utilizado foi o Rely XTM (3M, Sumaré, Brasil). A técnica preconizada pelo fabricante foi seguida rigorosamente: a dentina do canal radicular foi condicionada com ácido fosfórico a 37% por 15 segundos, lavada pelo mesmo período de tempo e seca, cuidadosamente, com papel absorvente. Sobre a dentina foi colocado um anel de plástico de 0,6mm de diâmetro e 8mm de altura, para padronizar a área que receberia a resina. Seguiu-se com a colocação do sistema adesivo na dentina radicular e com auxílio de pincel (Microbrush®, Grafton, EUA), utilizando o Single BondTM (3M, Sumaré, Brasil). O agente de cimentação resinoso RelyXTM (3M, Sumaré, Brasil) foi dispensado 1:1 sobre um bloco de papel impermeável e espatulado de acordo com as recomendações do fabricante. Ao final da espatulação, o agente resinoso foi posto em contato com a dentina radicular e, posteriormente, uma argola de metal fixado para o teste de tração. Em seguida, realizou-se a fotopolimerização por 20 segundos em cada face do cimento resinoso.
Ensaio de resistência à tração
Para a realização do ensaio de resistência à tração utilizou-se um conjunto de peças de metal, fabricado exclusivamente para essa metodologia, de modo que fixasse o bloco da dentina na máquina e permitisse a tração do cimento resinoso fixado na dentina através do anel de metal preso no cimento resinoso.
Os anéis foram fixados da máquina de ensaio EMIC regulada à velocidade de 0,5mm/minutos. A seguir, os resultados em quilograma força (Kgf) foram tabulados e submetidos à análise estatística.
Este estudo foi conduzido de acordo com os preceitos determinados pelo Colégio Brasileiro em Experimentação Animal e o projeto aprovado pelo Comitê de Ética em Pesquisa Animal do Centro de Pesquisa Odontológicas São Leopoldo Mandic (Protocolo nº1121).
RESULTADOS
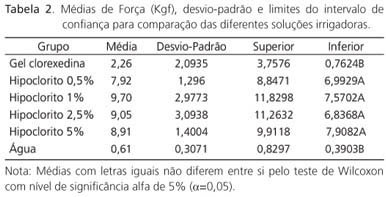
Os valores obtidos no ensaio de resistência à tração foram então submetidos à análise estatística (Tabela 1 e Figura 2).
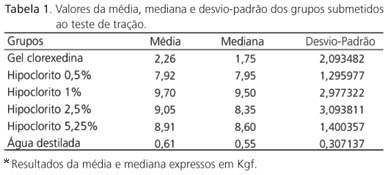
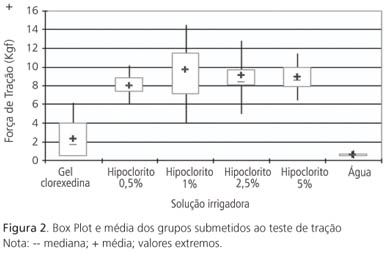
O Teste de Kruskall-Wallis mostrou fortes indícios (p<0,01) de que há efeito significativo das soluções irrigadoras sobre a Força.
O teste de Wilcoxon mostrou que as médias verdadeiras de Força das soluções irrigadoras com hipoclorito são significativamente maiores que as médias verdadeiras dos grupos irrigados com gel clorexidina e água (Tabela 2).
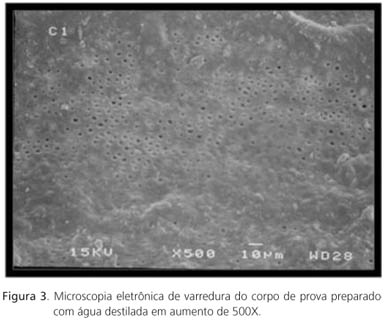
Avaliação da dentina através da microscopia eletrônica de varredura
As fotografias realizadas através da microscopia eletrônica de varredura com aumentos de 500X e 1500X registraram a superfície dentinária após condicionamento com diferentes soluções químicas. Pôde-se observar que o grupo tratado com água destilada (Figura 3) e gel de clorexidina apresenta uma superfície ampla de dentina intertubular e peritubular, com poucos canalículos dentinários expostos e de pequeno diâmetro. Para os grupos que receberam hipoclorito de sódio na concentração de 0,5% e 1% (Figura 4), observou-se uma superfície com menor área de dentina intertubular e peritubular. Assim, os diâmetros dos canalículos se apresentam mais amplos e em maior quantidade, além disso, observou-se pequenas depressões na superfície da dentina. Nas concentrações de 2,5% e 5,25% notou-se uma dentina com uma superfície altamente alterada, com pequena presença de dentina intertubular e peritubular, diâmetro dos túbulos dentinários aumentados e grandes depressões em toda estrutura.

DISCUSSÃO
A restauração final do dente tratado endodonticamente reflete todo procedimento realizado desde o diagnóstico, fundamental para o correto planejamento do tratamento, assim como acesso cirúrgico, preparo químico-mecânico e a obturação, pois estes fatores podem interferir no tipo de material restaurador utilizado, bem como a necessidade ou não de retentor intra-canal. Assim, é importante a estrutura remanescente do dente no planejamento da restauração final. Segundo Shillingburg et al.2, os dentes, que foram tratados endodonticamente e sofreram grande perda de estrutura dental sadia, necessitam, na maioria das vezes, da utilização de núcleo com pino radicular para retenção de coroa protética visto que a função essencial do pino é a de reter a prótese ou o material restaurador.
Asmussen et al.3 preconizaram a utilização de cimentos resinosos para fixação de retentores, pois apresentam função de estabilização do pino no interior da estrutura radicular e do selamento do espaço endodôntico.
Dessa forma, dependendo do tipo de retentor e do cimento de fixação que se utiliza, há a possibilidade de se encontrarem algumas variáveis que podem interferir na retenção do pino intra-radicular e na adesão do cimento resinoso. Entre esses fatores, são citados o cimento obturador dos sistemas de canais radiculares e os tipos de soluções químicas utilizadas durante o preparo dos sistemas de canais.
A dificuldade de realização de trabalhos com dentes humanos, frente ao Comitê de Ética em Odontologia, a dificuldade de padronização em relação à obtenção de dentes humanos, principalmente quando se pretende avaliar a interação das estruturas da dentina com sistemas adesivos, fez com que a amostra do presente estudo fosse composta por dentes bovinos, já que de acordo com Nakamichi & Fusayama et al.4, as estruturas dentais da família dos mamíferos são similares e, segundo Schilke et al.5 e Fonseca et al.6, a força de tração exigida tanto em dentina humana como em bovina não apresentaram diferença significativa quando avaliadas in vitro.
Além disso, por meio de microscopia eletrônica de varredura, as características físicas da dentina bovina são semelhantes à dentina humana, fato que foi descrito por Schmalz et al.7 e Reis et al.8. Esses autores concluíram que a dentina de ambos apresenta as mesmas estruturas morfológicas e que os dentes bovinos podem ser uma alternativa para trabalhos que visam observar a permeabilidade da dentina. Por isso, o presente estudo avaliou a interferência das soluções químicas na dentina bovina.
A utilização de soluções irrigadoras faz parte do preparo químico-mecânico da dentina: o preparo químico corresponde às propriedades químicas que as soluções irrigantes apresentam, e o mecânico corresponde à seqüência de instrumentação9.
Segundo Thé10 e Cunningham & Balekjan11, o hipo-clorito de sódio apresenta não só capacidade de dissolução de tecido orgânico, como também a capacidade de promover a lise proteica, liberar cloro na forma de gás e capacidade osmótica de retirar fluídos celulares, o que explica a capacidade solvente e antimicrobiana de tal solução.
Assim, no presente estudo as soluções químicas utilizadas foi o hipoclorito de sódio, pois preenche grande parte do perfil ideal para uma substância química.
O pH do hipoclorito de sódio utilizado foi determinado em 9,4 a temperatura de 25ºC, pois, segundo Siqueira12, o potencial de dissolução de tecido orgânico está relacionado nessa ordem: pH, temperatura e concentração. Para Spanó13, a variação do pH e a temperatura influenciam diretamente no potencial de dissolução das soluções de hipoclorito. Neste estudo, optou-se por manter esses fatores iguais para todos os grupos de hipoclorito de sódio, pois as pesquisas de alterações de pH e temperatura foram estudadas apenas in vitro, devendo ser mais bem estudadas in vivo para que se possam utilizar as soluções de hipoclorito com diferentes pH e temperatura.
Além das características antimicrobianas alteradas, segundo Okino et al.14 e Nakamura et al.15, a variação da concentração da solução de hipoclorito de sódio é importante, pois existe uma diferença na dissolução tecidual. De acordo com esses autores, sempre que se aumentou a concentração dessa solução, mantendo-se as mesmas propriedades físicas e químicas, a dissolução de tecido foi maior.
Neste trabalho, diferentes resultados foram observados na dentina radicular quando da variação das concentrações de hipoclorito de sódio. Após a utilização do hipoclorito de sódio a 0,5%, observou-se, em microscopia eletrônica de varredura, uma superfície dentinária com canalículos desobstruídos superior ao grupo em que se utilizou água destilada. Na concentração de hipoclorito de sódio a 1%, observa-se uma superfície com maior número de canalículos mais amplos, além de uma superfície dentinária com irregularidades. Nas concentrações de 2,5% e 5,25%, observam-se uma dentina com uma superfície com depressões em toda sua estrutura, além de túbulos dentinários maiores e mais amplos.
Outra substância química utilizada durante o preparo dos espécimes foi o EDTA a 17%, pois segundo Goldman et al.1 o hipoclorito de sódio produz uma dentina limpa, removendo apenas o material orgânico. Yamada et al.16 afirmaram que não há uma solução química ideal e que deve existir uma combinação de diferentes soluções para que ocorra uma maior efetividade na dentina.
Durante o preparo biomecânico dos sistemas de canais radiculares, formam-se resíduos de dentina, restos teciduais e bacterianos. Esses resíduos formados são chamados de smear layer ou magmas residuais, que se aderem à superfície da dentina e podem conter micro-organismos viáveis que colonizam os túbulos dentinários.
Ruse & Smith17 comprovaram que a presença de magma residual nas paredes dos canais radiculares impede que o material obturador penetre nos túbulos dentinários e preconizam a remoção total desse esfregaço, pois se acredita que ocorram micro-retenções no interior dos canais aumentando a retenção mecânica. Assim, a remoção dessa lama dentinária deve ser realizada com soluções ácidas.
Dentre as soluções utilizadas, o EDTA tem sido a solução química com melhor atuação na remoção da smear layer1,16.
Eldeniz et al.18 demonstraram que o pré-tratamento da dentina radicular com EDTA a 17% e hipoclorito de sódio a 5,25% influencia, positivamente, na força de adesão para o cimento obturador resinoso AH plus (Dentsply, Chicago, EUA).
Assim, no presente estudo, utilizou-se EDTA 17% após preparo com o hipoclorito de sódio e gel de clorexidina, no entanto, Saleh & Ettman19 ressaltaram que a utilização dessa solução pode provocar um decréscimo na massa dentinária e diminuir, assim, a microdureza da dentina.
As soluções químicas descritas apresentam algumas propriedades químicas desfavoráveis como a irritação dos tecidos periapicais. Por isso, tem se buscado a utilização de soluções químicas que não apresentem essa característica. O digluconato de clorexidina aparece como uma alternativa para a solução, conforme relataram Jeansonne & White 20.
A principal característica do digluconato de clorexidina é o seu potencial antimicrobiano relatados por Gomes et al.21 e Spratt et al.22 e frente a micro-organismos do biofilme apical
Todavia, as características de uma solução química irrigadora não se limitam apenas em ser um potente antimicrobiano, a dissolução tecidual também é um fator de grande importância na escolha do agente irrigante9.
Siqueira12 relata que o gel de clorexidina a 2% não dissolveu tecido orgânico durante o tempo experimental de 120 minutos. Okino et al.14 demonstraram que as preparações de hipoclorito de sódio apresentam a capacidade de dissolução tecidual, variando apenas o tempo de contato. Neste estudo observou-se nas imagens produzidas pela microscopia eletrônica de varredura que a dentina tratada com gel de clorexidina apresentou ampla superfície de dentina intertubular e peritubular e com poucos canalículos dentinários expostos. Isto se deve ao fato que a clorexidina não apresenta capacidade de dissolução de matéria orgânica, constituinte da dentina intertubular e peritubular e assim a atuação do EDTA não atua conjuntamente, pois a não remoção da superfície orgânica não permite a penetração adequada do EDTA.
Dadas as propriedades físico-químicas do hipoclorito de sódio e da clorexidina como substâncias químicas auxiliares no preparo bio-mecânico, a avaliação das consequências que essas soluções podem provocar na restauração final do elemento dental, quando se utiliza material resinoso, é necessária, já que esses cimentos se unem à dentina química e mecanicamente23-24.
O teste de tração utilizado nesta pesquisa, representa em KgF a força necessária para remover o cimento resinoso da dentina tratada previamente. Reis et al.8 e Utter et al.25 utilizaram esse tipo de teste para avaliação dos seus experimentos.
Observou-se no presente trabalho que o tratamento com hipoclorito de sódio influenciou nos resultados para os testes de tração. A análise estatística também revelou uma conformidade dos resultados em relação às diferentes concentrações de hipoclorito de sódio utilizados. O gel de clorexidina não teve influência na adesão quando comparado com o grupo da água destilada, devido ao fato da não exposição de uma superfície radicular com canalículos expostos e áreas de retenção e penetração de resina.
No presente estudo utilizou-se cimento resinoso Rely XTM (3M, Sumaré, Brasil), pois este agente fixador apresentou bom comportamento em comparação com cimentos à base de fosfato de zinco e ionômero de vidro, na cimentação de retentor intra-radicular26.
Vargas et al.27 avaliaram a influência do hipoclorito de sódio na adesão da resina em dentina, o que não apresentou diferença estatística na força de adesão, e, na avaliação microscópica, observaram que a camada de colágeno fora removida. De acordo com os autores, o colágeno pode não ser crucial na adesão entre resina e dentina e também que as fibras colágenas podem inibir a penetração de resina no substrato dentinário; pois, quando se remove o colágeno, ocorre uma maior difusão do adesivo na dentina.
Nesta pesquisa, observou-se em microscopia eletrônica de varredura que o tratamento da superfície dentinária pelo hipoclorito de sódio, promoveu uma grande abertura dos túbulos e deixou os canalículos mais amplos, com menor quantidade de dentina intertubular, com maior área de contato entre a dentina e a resina foi estabelecida, assim os resultados obtidos nos testes de tração foram maiores para o hipoclorito de sódio.
Reis et al.8 também observaram que a resistência à tração não está relacionada à formação da camada híbrida, pois a remoção do colágeno promoveu espaços na dentina fazendo com que ocorressem mais tags, aumentando, assim, o embricamento mecânico, e o aumento da resistência, o que formou uma camada híbrida reversa. Esses achados corroboram com os encontrados no presente estudo, em que a força de tração necessária para remoção da resina da dentina, em que se utilizou o hipoclorito de sódio, foi maior estatisticamente do que para os grupos em que se utilizaram gel de clorexidina e água destilada.
Alguns relatos apresentados na literatura são diferentes do observado neste estudo. Ozturk & Ozer24 e Perdigão et al.28 avaliaram a influência do hipoclorito de sódio na dentina, por diferentes períodos de tempo e concluíram a ocorrência de um decréscimo na força de adesão. Isto deve-se, principalmente, pela metodologia utilizada pelos autores, que utilizaram altas concentrações de hipoclorito de sódio por períodos curto de tempo. Além disso, a dentina estudada por estes autores difere do presente estudo, pois foi utilizada próxima ao limite do esmalte, com características de menor quantidade de canalículos, além de túbulos mais estreitos29. Assim, os resultados obtidos diferem do presente estudo, que avaliou uma dentina próxima a cavidade pulpar, além do maior tempo de contato e menor concentração das soluções químicas.
Morris et al.30 obtiveram resultados diferentes, em que o hipoclorito de sódio ao atuar em dentina, interferiu na adesão e causou um decréscimo na força de tração.
Vale ressaltar que a literatura se apresentou escassa quanto à avaliação da dentina após preparo químico endodôntico, sendo estudada apenas na área da dentistíca em que se utiliza o hipoclorito de sódio em altas concentrações, em pequenos períodos de tempo.
Dessa forma, pode-se inferir que a utilização do hipoclorito de sódio, que apresenta capacidade de dissolução tecidual, interfere, positivamente, na adesão à dentina quando utilizado de acordo com a técnica proposta neste trabalho.
É indispensável a avaliação de outras condições quanto ao tempo de atuação, ao contato mecânico com a dentina e outros tipos de sistemas adesivos existentes, bem como de cimentos de fixação.
CONCLUSÃO
De acordo com a metodologia empregada e os resultados obtidos, pode-se concluir que o hipoclorito de sódio nas concentrações testadas aumenta a força de adesão do cimento resinoso na dentina de forma significativa frente água destilada e gel de clorexidina a 2%, em teste de tração.
Colaboradores
GR CAMPOS e RJA CARDOSO foram os responsáveis pelo desenvolvimento da pesquisa e pela análise de interpretação dos dados, bem como na organização final da mesma. MCP SILVA contribuiu no desenvolvimento da metodologia mais especificadamente na obtenção das imagens em microscopia eletrônica de varredura e auxilio na interpretação dos resultados e discussão.
REFERÊNCIAS
1. Goldman M, DeVitre R, White R, Nathanson D. An SEM Study of posts Cemented with an Unfilled Resin. J Dent Res. 1984;63(12):1003-5. [ Links ]
2. Shillingburg HT, Kessler JC. Restoration of endodontically treated tooth. Chicago: Quintessence Pub. Co., 1982. [ Links ]
3. Asmussen E, Peutzfeldt A, Heitmann T. Stiffness, elastic limit, and strength of newer types of endodontic posts. J Dent. 1999;27(4):275-8. [ Links ]
4. Nakamichi MI, Fusayama T. Bovine teeth as possible substitutes in the adhesion test. J Dent Res. 1963;62(10):1076-81. [ Links ]
5. Schilke R, Bauss O, Lisson JA, Schuckar M, Geurtsen W. Bovine dentin as a substitute for human dentin in shear bond strength measurements. Am J Dent. 1999;12(2):92-6. [ Links ]
6. Fonseca RB, Haiter-Neto F, Fernandes-Neto AJ, Barbosa GA, Soares CJ. Radiodensity of enamel and dentin of human bovine and swine teeth. Arch Oral Biol. 2004;49(11):919-22. [ Links ]
7. Schmalz G, Hiller KA, Nunez LJ, Stoll J, Weis K. Permeability characteristics of bovine and human dentin under different pretreatment conditions. J Endod. 2001;27(1):23-30. [ Links ]
8. Reis A, Bozzo A, Bocangel JS. Influência do colágeno na resistência de união à dentina úmida e seca. RPG Rev Pos-Grad. 2000;7(2):133-9. [ Links ]
9. Pécora JD, Souza Neto MD, Estrela C. Substâncias químicas auxiliares. In: Estrela C, Figueiredo JAP. Endodontia: princípios biológicos e mecânicos. São Paulo: Artes Médicas; 1999. p.551-70. [ Links ]
10. Thé SD. The solvent action of sodium hipochlorite on fixed and unfixed necrotic tissue. Oral Surg Oral Med Oral Pathol. 1979;47(6):558-61. [ Links ]
11. Cunningham WT, Balekjian AY. Effect of temperature on collagen-dissolving ability of sodium hypochlorite endodontic irrigant. Oral Surg. 1980;49(2):175-7. [ Links ]
12. Siqueira EL. Dissolução de tecido pulpar bovino por duas substâncias químicas auxiliares da instrumentação [tese]. São Paulo: Universidade de São Paulo; 2004. [ Links ]
13. Spanó JCE. Estudo in vitro das propriedades físico-químicas das soluções de hipoclorito de sódio, em diferentes concentrações, antes e após a dissolução de tecido pulpar bovino [tese]. Ribeirão Preto: Universidade de São Paulo; 1999. [ Links ]
14. Okino LA, Siqueira EL, Santos M, Bombana AC, Figueiredo JA. Dissolution of pulp tissue by aqueous solution of chlorhexidine digluconate and chlorhexidine digluconate gel. Int Endod J. 2004;37(1):38-41. [ Links ]
15. Nakamura H, Asai K, Fujita H, Nakazato H, Nishimura Y, Furuse Y, et al. The solvent action of sodium hypochlorite on bovine tendon collagen, bovine pulp, and bovine gingiva. Oral Surg Oral Med Oral Pathol. 1985;60(3):322-6. [ Links ]
16. Yamada RS, Armas A, Goldman M, Lin PS. A scanning electron microscopic comparison of a high volume final flush with several irrigating solutions: part 3. J Endod. 1983;9(4):137-42. [ Links ]
17. Ruse ND, Smith DC. Adhesion to bovine dentin-surface characterization. J Dent Res. 1991;70(6):1002-8. [ Links ]
18. Eldeniz AU, Erdemir Al, Belli S. Shear bond strength of three resin based sealers to dentin with and without the smear layer. J Endod. 2005;31(4):293-6. [ Links ]
19. Saleh AA, Ettman WM. Effect of endodontic irrigation solutions on microhardness of root canal dentin. J Dent. 1999;27(1):43-6. [ Links ]
20. Jeansonne MJ, White RR. A comparasion of 2,0% chlorexidine gluconate and 5,25% sodium hipoclorite as antimicrobial endodontics irrigants. J Endod. 1994;20(6):276-8. [ Links ]
21. Gomes BP, Ferraz CC, Vianna ME, Berber VB, Teixeira FB, Souza-Filho FJ. In vitro antimicrobial activity of several concentrations of sodium hypoclorite and clorhexidine gluconate in the elimination of Enterococcus faecalis. Int Endod J. 2001;34(6):424-8 [ Links ]
22. Spratt DA, Pratten J, Wilson M, Gulabivala K. An in vitro evaluation of the antimicrobial efficacy of irrigants of root canal isolates. Int End J. 2001;34(4):300-7. [ Links ]
23. Sinhoretti MAC, Góes MF, Consani S. Resistência ao cisalhamento da União de sistemas adesivos sobre dentina. Rev Assoc Paul Cir Dent. 1997;51(3):15-20. [ Links ]
24. Ozturk B, Ozer F. Effect of NaOCl on bond strengths of bonding agents to pulp chamber lateral walls. J Endod. 2004;30(5):362-5. [ Links ]
25. Utter JD, Wong BH, Miller BH. The effect of cementing procedures on retention of prefabricated metal posts. J Am Dent Assoc. 1997;128(8):1123-7. [ Links ]
26. Sigemori RM, Reis AF, Giannini M, Paulillo LA. Curing depth of a resin-modified glass ionomer and two resin-based luting agents. Oper Dent. 2005;30(2):185-9. [ Links ]
27. Vargas MA, Cobb DS, Armstrong SR. Resin-dentin shear bond strength and interfacial ultrastructure with and without a hybrid layer. Oper Dent. 1997;22(4):159-66. [ Links ]
28. Perdigão J, Lopes M, Geraldeli S, Lopes GC, García-Godoy F. Effect of a sodium hypochlorite gel on dentin bonding. Dent Mater. 2000;16(5):311-23. [ Links ]
29. Bhaskar SN. Histologia e embriologia oral de Orban. 10ª ed. São Paulo: Artes Médicas; 1992. p.111-45 [ Links ]
30. Morris MD, Lee KW, Agee KA, Bouillaguet S, Pashley DH. Effects of sodium hypochlorite and rc-prep on bond strengths of resin cement to endodontic surfaces. J Endod. 2001;27(12):753-7. [ Links ]
Recebido em: 17/12/2009
Versão final reapresentada em: 25/7/2010
Aprovado em: 14/9/2010
* Correspondência para / Correspondence to: MCP SILVA. E-mail: <marcaven@gmail.com>.