Serviços Personalizados
Artigo
Links relacionados
Compartilhar
RSBO (Online)
versão On-line ISSN 1984-5685
RSBO (Online) vol.8 no.4 Joinville Out./Dez. 2011
TÓPICOS DA ODONTOLOGIA
DENTISTRY TOPICS
Alterações pulpares e periapicais
Pulp and periapical pathologies
Denise Piotto LeonardiI; Allan Fernando GiovaniniI; Susimara AlmeidaI; Celso Alfredo SchrammI; Flares Baratto-FilhoI
I Mestrado profissional em Odontologia Clínica, Universidade Positivo – Curitiba – PR – Brasil
RESUMO
A polpa, diante de um fator agressor, apresenta reações inflamatórias ou degenerativas. Estas dependem do tipo, da frequência e da intensidade do agente irritante, assim como da resposta imune do paciente. Se o agente agressor não for removido, a polpa alterada ficará calcificada ou necrosada. Quando uma alteração pulpar está presente e não é tratada, poderá evoluir para a necrose pulpar. A necrose pulpar consiste na completa cessação dos processos metabólicos do tecido pulpar e, se não for removida, os produtos tóxicos bacterianos e da decomposição tecidual vão agredir os tecidos periapicais, dando início às alterações periapicais. O profissional deve ter conhecimento sobre as características histológicas, clínicas e radiográficas dessas patologias para poder reconhecê-las e indicar a melhor opção de tratamento.
Palavras-chave: polpa dentária; tecidos periapicais; patologia.
ABSTRACT
The pulp undergoes inflammatory or degenerative reactions when submitted to an aggressive factor. These depend on the type, frequency and intensity of the irritant as well as the patient's immune response. If the aggressive agent is not removed, the pulp will either show calcifications or result in necrosis. This latter would occur when a pulp alteration is present and not treated. Pulp necrosis is the complete cessation of the tissue's metabolic processes. If it is not removed, the bacterial and the tissue decomposition's toxic products will injure the periapical tissues, resulting in periapical alterations. The dentist must know the histological, clinical and radiographic features of these pathologies to recognize them and indicate the best treatment option.
Keywords: dental pulp; periapical tissue; pathology.
Alterações pulpares
A polpa dental é um tecido conjuntivo frouxo encontrado no interior da cavidade pulpar (câmara pulpar e canal radicular) que contém grande número de vasos sanguíneos, vasos linfáticos, fibras nervosas e células. Entre estas, estão os odontoblastos, os quais diferenciam o tecido pulpar dos demais tecidos conjuntivos presentes em outras regiões do corpo.
Por possuir um metabolismo intenso, a polpa dental apresenta boa capacidade de reparo. Por ser um tecido conjuntivo, quando diante de um agente agressor ocorrem fenômenos vasculoexsudativos, caracterizando a inflamação. Em virtude de a polpa dental estar circundada por paredes dentinárias rígidas, quando ocorrem a inflamação pulpar e, consequentemente, o aumento de volume desse tecido, há a compressão de fibras nervosas, gerando dor. Além disso, o aumento do volume pulpar pode dificultar a circulação sanguínea local e o retorno de sangue venoso via forame apical, o que prejudica a capacidade de defesa do tecido pulpar.
Fatores locais e sistêmicos interferem na intensidade da resposta pulpar diante de um agente agressor. Como exemplos de fatores locais citam-se o número e a virulência dos microrganismos presentes no tecido cariado. O fator sistêmico é representado pela resposta imune do paciente. Quando os agentes etiológicos excedem o limiar de tolerância pulpar, instalam-se as patologias pulpares.
Agentes agressores ao tecido pulpar
Agentes químicos
São representados pelos materiais odontológicos que, aplicados em cavidades profundas (por exemplo, os adesivos dentinários) sem a devida proteção do complexo dentinopulpar, podem atuar como fator irritante ao tecido pulpar, levando à sua inflamação.
Agentes biológicos
Os fatores biológicos são representados pelos microrganismos presentes na cárie dental ou em periodontopatias. Se a cárie dental não for tratada, as bactérias ali presentes agridem o tecido pulpar via túbulos dentinários. Em casos de periodontopatias, como, por exemplo, em abscessos periodontais, as bactérias poderão agredir a polpa dental através das vias de intercomunicação polpa/periodonto.
A fratura dental com exposição de dentina ou dentina/polpa aos microrganismos da cavidade bucal também representa um fator biológico à alteração pulpar.
Agentes físicos
Os fatores físicos podem ser representados pelo uso de brocas em alta rotação sem adequada refrigeração durante o preparo de cavidades na dentística restauradora.
A polpa de dentes acometidos por bruxismo, erosão, abrasão e atrição também está diante de fator agressor físico.
A formação de correntes elétricas (galvanismo), por causa da presença de restaurações metálicas, agride o tecido pulpar.
Reações pulpares ante a ação de agentes agressores
A polpa, por ser um tecido conjuntivo, quando diante de um fator agressor responderá por meio de reações de defesa. Tais reações podem ser inflamatórias ou degenerativas e vão estar presentes dependendo do tipo, da frequência e da intensidade do agente irritante. Fatores sistêmicos também influenciam no tipo de resposta pulpar ante o agente patogênico. Se essas reações não forem interrompidas por intermédio da remoção da causa (por exemplo, remoção de cárie e tratamento restaurador), a polpa caminhará para o envelhecimento pulpar e a calcificação do canal radicular ou para as pulpites e a necrose pulpar..
Alterações pulpares degenerativas
• Formação de dentina reacional: no mesmo local acometido pela cárie, mas na superfície interna, podem ser observadas deposição de dentina reacional e, por conseguinte, redução do volume da polpa coronária e alteração da câmara pulpar. A dentina reacional é depositada à medida que a cárie invade o tecido dentinário;
• Esclerose dentinária: é representada pela diminuição do diâmetro dos túbulos dentinários em decorrência da deposição de dentina peritubular. A diminuição da luz dos túbulos faz com que a proteção gerada pelo f luido dentinário seja diminuída, pois há pouco espaço para o movimento do fluido;
• Tratos mortos da dentina: ocorrem quando os prolongamentos dos odontoblastos se retraem, deixando os túbulos dentinários vazios e sem proteção, favorecendo a invasão de bactérias da cárie e a agressão ao tecido pulpar;
• Envelhecimento pulpar: redução da capacidade de defesa do tecido pulpar pela diminuição do número de células, vasos e nervos (figura 1);
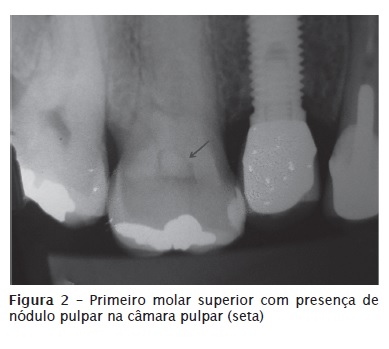
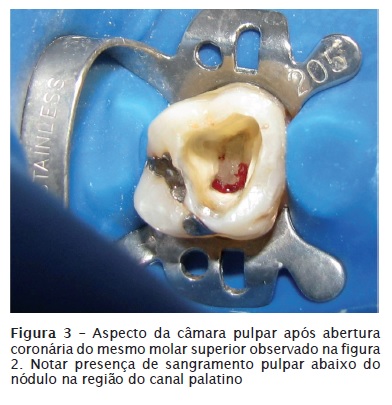
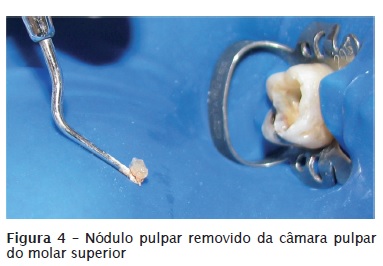
• Formação de áreas de hialinização: sobre elas poderá ocorrer deposição de tecido mineralizado, dando origem aos nódulos pulpares (figuras 2, 3 e 4).

Alterações pulpares inflamatórias
De acordo com a intensidade do agente agressor e a resposta imune do paciente, alterações inflamatórias poderão acometer o tecido pulpar. Dessa forma, as reações inflamatórias pulpares são de caráter agudo ou crônico. A alteração pulpar aguda é denominada de pulpite aguda, enquanto a alteração pulpar crônica recebe o nome de pulpite crônica. Ressalta-se que alterações inflamatórias apenas acometem o tecido conjuntivo vivo. Portanto, a polpa apresenta-se com vitalidade quando diante dos diferentes estágios de inflamação.
Como a principal característica clínica das alterações pulpares inflamatórias é a presença de dor, antes de descrever os diferentes tipos de pulpites é importante expor as características clínicas da dor de origem pulpar.
Características clínicas da dor de origem pulpar
A dor de origem pulpar pode ser classificada quanto à natureza, intensidade, frequência, localização e qualidade.
No que se refere à natureza, a dor pulpar pode ser provocada ou espontânea. É provocada quando o processo inflamatório está em estágio inicial e espontânea quando o processo já está avançado. Para a compreensão por parte do paciente, deve-se fazer a seguinte pergunta: Seu dente dói sozinho ou precisa de estímulo para que ocorra a dor?
No tocante à intensidade, a dor pulpar pode ser leve, moderada ou forte. É possível pedir ao paciente para classificar de 0 a 10 a intensidade da dor que está sentindo; quanto maior a intensidade, mais avançado está o processo inflamatório.
Quanto à frequência, a dor pode ser intermitente ou contínua, ou seja, ela pode aparecer em intervalos ou, quando desencadeada, demorar para passar.
Caso a dor seja localizada, o paciente consegue indicar exatamente qual dente causa dor; se for difusa (ou reflexa), o paciente relata que a região está dolorida e não determina, ao certo, o dente originário de dor. Ele pode dizer que sente dores que se iniciam no dente e irradiam para outros dentes da mesma arcada, ou da arcada antagonista ou para regiões como cabeça, ouvido, pescoço. Quando a dor difusa está presente, isso denota uma alteração patológica mais avançada.
No que respeita à qualidade da dor, pode ser pulsátil (latejante) ou não. Tal tipo de dor se apresenta em pulpites mais avançadas.
Pulpites agudas
As pulpites agudas são classificadas clinicamente, de acordo com o grau de comprometimento pulpar, em reversível, reversibilidade duvidosa e irreversível. Ressalva-se que as alterações pulpares não são observadas radiograficamente.
O exame radiográfico vai apenas mostrar se há presença de cáries ou restaurações profundas, que podem ser a causa da alteração pulpar. Na região periapical não se observa presença de lesão, e sim espaço periodontal apical normal ou levemente aumentado, mas com lâmina dura normal.
Pulpite aguda reversível
Neste estágio inicial de inflamação, a polpa está sob agressão; todavia, se o agente patogênico for removido, apresenta condições de voltar ao estado de normalidade. Clinicamente, o paciente acusa dor aguda, provocada muitas vezes pelo frio ou pelo doce, de curta duração que passa rápido após a remoção do estímulo. O prognóstico para o dente e para o tecido pulpar, nessa condição, mostra-se favorável. O tratamento indicado é o conservador, ou seja, a remoção do agente agressor ou proteção pulpar indireta ou direta.
É importante diferenciar a pulpite aguda reversível de hipersensibilidade dentinária. Esta pode estar presente em casos de exposição dentinária cervical, na qual o estímulo térmico ou mecânico (por exemplo, a escovação) gera dor; para tratamento recomenda-se restauração da cavidade.
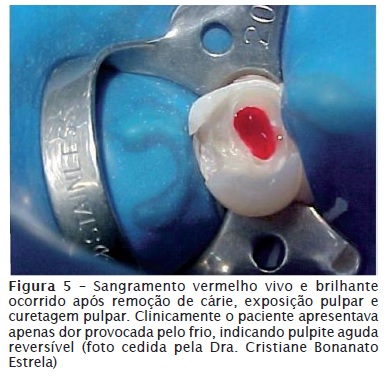
Macroscopicamente, se fosse possível observar a polpa inflamada reversivelmente, seu aspecto seria de sangramento vermelho vivo e brilhante (figure 5), polpa com consistência e resistente ao corte.
Pulpite aguda de reversibilidade duvidosa
Tal alteração pulpar evidencia características de pulpite aguda reversível e de pulpite aguda irreversível, denotando um estado inflamatório transicional entre esses dois tipos de alteração. O prognóstico da polpa nessa condição é incerto, pois depende do tempo que a polpa está sob agente agressor. Também deve ser considerado o risco de a inflamação ter comprometido irreversivelmente a polpa, mas ainda existirem algumas características clínicas de pulpite aguda reversível.
O paciente pode relatar dor espontânea, intermitente, provocada pelo frio, e demora para passar após a remoção do estímulo; a dor pode ser aliviada por analgésicos comuns.
Diante de tal condição pulpar, realiza-se tratamento conservador. No entanto é importante deixar claros para o paciente o risco de evolução para uma pulpite aguda irreversível e a necessidade de tratamento endodôntico.
Pulpite aguda irreversível
Esta condição pulpar denota estágio avançado de inflamação. A polpa está sob agressão, e apenas a remoção do agente patogênico não basta para cessar a dor, ou seja, a polpa não apresenta condições de voltar ao estado de normalidade após a remoção da causa.
Clinicamente, o paciente acusa dor aguda, espontânea, intensa, pulsátile, quando desencadeada, demora de segundos a horas para aliviar. Analgésicos, nem os mais potentes são capazes de aliviar a dor. No exame radiográfico a pulpite aguda irreversível não mostra sinais. A região periapical, radiograficamente, pode estar normal ou com aumento do espaço periodontal apical e lâmina dura intacta.
Quando a pulpite aguda irreversível se encontra em estágio inicial, o paciente ainda pode conseguir localizar o dente, facilitando o diagnóstico por meio de teste de vitalidade que acusará dor exacerbada. Por outro lado, se a inflamação irreversível progride, a dor passa a ser difusa ou reflexa (irradiada para outros dentes ou regiões da cabeça), exacerbada pelo calor e aliviada com o frio. Nesse estágio, o paciente pode relatar que compressas com gelo aliviam a sintomatologia dolorosa.
Na pulpite aguda irreversível é comum o paciente afirmar que a dor fica mais intensa à noite. Isso ocorre pelo fato de, ao deitar-se, a pressão interna pulpar aumentar; como o tecido se encontra inflamado, a dor é exacerbada.
Nessa condição, o prognóstico para o dente mostra-se favorável; já para o tecido pulpar é desfavorável, e então a polpa deve ser removida. O tratamento indicado é o endodônt ico – a biopulpectomia.
Macroscopicamente, quando acessada, a polpa demonstra as seguintes características: sangramento discreto e com coloração vermelho escuro e opaco, consistência pastosa e sem resistência ao corte.
Pulpites crônicas
As alterações pulpares crônicas são observadas, geralmente, em dentes de pacientes jovens, haja vista sua incidência estar relacionada à presença de agentes agressores de baixa intensidade em contato com a polpa jovem, a qual apresenta elevada resistência imune. Na pulpite crônica, a polpa não está mais circundada em todos os lados por tecido duro, pois a cárie profunda permite uma exposição pulpar, mesmo que mínima, levando a um contato da polpa com a cavidade oral. Desse modo, os produtos tóxicos bacterianos e os mediadores químicos da inflamação não estão mais confinados e fechados na cavidade pulpar, como ocorre nas alterações pulpares agudas. Na pulpite crônica, a comunicação entre polpa e cavidade oral leva à diluição desses produtos tóxicos, diminuindo seu efeito deletério ao tecido pulpar.
A pulpite crônica é classificada em crônica ulcerada e crônica hiperplásica.
Pulpite crônica ulcerada
A pulpite crônica ulcerada é caracterizada pela presença de ulceração, visível microscopicamente, na superfície pulpar em contato com o meio bucal.
Clinicamente, o paciente relata dor provocada durante a mastigação em dentes com cáries profundas ou restaurações profundas mal adaptadas. Radiograficamente, pode ser observada cárie ou restauração profunda e mal adaptada em contato com o tecido pulpar.
A escolha do tratamento dependerá das características do tecido pulpar abaixo da área ulcerada. Se abaixo da superfície ulcerada a polpa se apresentar com características macroscópicas de polpa saudável (semelhante às características da pulpite aguda reversível), deverá ser realizado o tratamento conservador da polpa, sobretudo se o dente tiver ápice incompleto. Isso porque o sucesso do tratamento pulpar conservador está relacionado ao reparo do paciente; em jovens a capacidade de defesa é maior.
Pulpite crônica hiperplásica
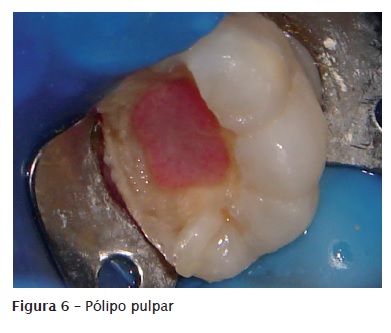
A principal característica da pulpite crônica hiperplásica é a presença do pólipo pulpar, visto clinicamente (figure 6). O pólipo pulpar representa a proliferação de tecido de granulação na superfície pulpar exposta à cavidade oral que, anteriormente à formação hiperplásica, estava ulcerada. Esse tipo de alteração pulpar é mais comum em dentes jovens, com ápice incompleto, por causa da capacidade de defesa aumentada. O trauma constante de alimentos e da mastigação sobre a superfície pulpar ulcerada leva à formação do pólipo pulpar.
O paciente relata dor provocada durante a mastigação e, clinicamente, é notado sangramento ao toque do pólipo, já que se trata de estrutura ricamente vascularizada. Radiograficamente, observa-se comunicação entre cavidade oral e cavidade pulpar por meio de cárie extensa e profunda. O tratamento para dentes com ápice completo com pulpite crônica hiperplásica é a biopulpectomia. Já para dentes com ápice incompleto, recomenda-se a manutenção da polpa radicular a fim de permitir a complementação radicular. Dessa forma, em dentes com ápice incompleto, sugere-se tratamento conservador denominado pulpotomia.
Alterações pulpares – considerações finais
É importante ressaltar que, seja qual for a fase em que se encontra a cárie, alterações inflamatórias do tecido pulpar podem ocorrer e estão relacionadas à intensidade do agente agressor e à capacidade de defesa do hospedeiro. Na maioria dos casos, o fator etiológico da patologia pulpar é biológico, ou seja, a cárie. No entanto não devem ser esquecidos os demais fatores, como os químicos e os físicos.
Diante de uma alteração pulpar, no momento da decisão do tipo de tratamento a ser realizado é preciso questionar se a polpa tem condições de ser mantida no interior da cavidade pulpar. Para isso, ao profissional cabe não apenas conhecer as características clínicas de cada tipo de patologia pulpar, como também saber classificá-las para, assim, ter condições de conferir o diagnóstico correto e, por conseguinte, indicar a melhor opção de tratamento.
Uma alteração pulpar não tratada vai evoluir para necrose pulpar. A necrose pulpar consiste na completa cessação dos processos metabólicos do tecido pulpar e, se não for removida do interior do canal radicular, ou seja, se não for feita a necropulpectomia, os produtos tóxicos bacterianos e da decomposição tecidual vão agredir os tecidos que estão em íntimo contato com o canal radicular, via forame apical – os tecidos periapicais –, dando início às periapicopatias ou alterações periapicais.
Alterações periapicais
Como consequência da cárie não removida ou de outros agentes causadores das alterações pulpares, ocorrerão necrose e, então, infecção pulpar. A microbiota em infecção pulpar é composta por bactérias aeróbias em processos iniciais e por anaeróbias nos processos mais avançados, predominando os microrganismos gram-negativos. Até o ano de 1970 acreditava-se que a microbiota endodôntica era composta por bactérias aeróbias. Todavia, já na década de 70, graças ao surgimento de técnicas anaeróbias de colheita bacteriana, notou-se grande presença de anaeróbios estritos no interior de canais radiculares. Até 1970 pensava-se que as espécies microbianas que ficavam isoladas no canal radicular após a necrose pulpar eram predominantemente aeróbias, visto que as técnicas de cultura bacterianas se caracterizavam por ser estritamente aeróbias.
A necrose pulpar, que representa a interrupção dos processos metabólicos da polpa com perda estrutural do tecido, permitirá a invasão bacteriana no canal radicular, provocando a resposta imune nos tecidos periapicais, os quais estão em íntimo contato com o canal radicular pelo forame apical. Logo após a necrose do tecido pulpar, a presença de bactérias restringe-se apenas à luz do canal principal.
Dependendo do agente causador da necrose pulpar, esta pode ser classificada em:
• Necrose por liquefação: é mais comum quando o agente agressor é bacteriano. Nesses casos, há uma interação dos microrganismos presentes com os neutrófilos; estes fagocitam e digerem as bactérias liberando enzimas proteolíticas que causam a degradação tecidual;
• Necrose por coagulação: ocorre quando há redução ou bloqueio do suprimento sanguíneo de um determinado tecido, levando à coagulação proteica tecidual. É comum tal tipo de necrose em casos de traumatismo dental – como luxação e intrusão –, que ocasiona rompimento do feixe vasculonervoso apical e consequente isquemia do tecido pulpar.
Com a instalação de um agente etiológico no interior do canal radicular, independentemente de sua natureza, a primeira região a sofrer agressão é a periapical. De início há uma reação de defesa (inflamação aguda) desses tecidos, denominada pericementite apical aguda. Desse modo, ocorrem fenômenos vasculoexsudativos com o aumento da permeabilidade vascular e exsudação plasmática para os espaços teciduais, formando edema na região periapical. Com a inflamação e a formação de edema na região periapical, acontece uma discreta extrusão dentária. Assim, clinicamente, há a sensação de "dente crescido" e dor à percussão vertical em casos de inflamação aguda dos tecidos periapicais. Os agentes etiológicos das alterações periapicais são classificados em biológicos, químicos e físicos:
• Agentes biológicos: necro se pulpar, periodontopatias, presença de bactérias no canal radicular em virtude da quebra de cadeia asséptica durante o tratamento endodôntico;
• Agentes químicos: soluções irrigadoras enérgicas, como hipoclorito de sódio em altas concentrações (4-6%), ou medicamentos agressivos, como tricresol formalina, empregados em casos de biopulpectomia, em que o tecido periapical se encontra com vitalidade. O extravasamento de cimento endodôntico para a região periapical também pode atuar como um agressor químico, dependendo de sua composição química;
• Agentes físicos: ocorrência de sobreinst rumentação, em que os inst rumentos endodônt icos são erroneamente usados, ultrapassando o limite apical do canal radicular e traumatizando os tecidos periapicais.
As patologias periapicais são classificadas em agudas ou crônicas.
Patologias periapicais agudas
• Pericementite apical aguda;
• Abscesso dentoalveolar agudo;
• Abscesso dentoalveolar crônico reagudizado (abscesso fênix).
Patologias periapicais crônicas
• Abscesso dentoalveolar crônico;
• Granuloma periapical;
• Cisto periapical.
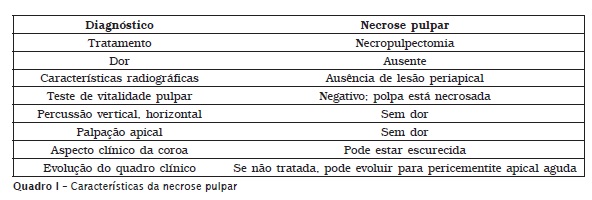
Os quadros I e II trazem, respectivamente, as características de necrose pulpar e de pericementite apical aguda.
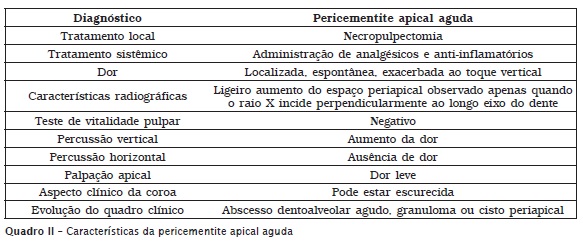
Como consequência da pericementite apical, podem ocorrer fenômenos periapicais agudos ou crônicos. Antes de evoluir para um processo inf lamatório crônico, a pericementite apical, inicialmente aguda, torna-se crônica. Clinicamente, a pericementite apical crônica não apresenta sintomatologia dolorosa e, radiograficamente, são observados aumento do espaço periapical, espessamento da lâmina dura e trabeculado ósseo apical mais denso.
Os fatores locais e sistêmicos determinam se a evolução da pericementite apical será para um processo inflamatório de caráter exsudativo (abscesso dentoalveolar agudo) ou proliferativo (granulomas e cistos).
• Fatores locais: número e virulência das bactérias, diâmetro do forame apical;
• Fatores sistêmicos: resistência orgânica.
As alterações de caráter exsudativo acontecerão quanto maior for o número e a virulência das bactérias e quanto mais baixa estiver a resistência orgânica ou resposta imune do paciente. Já as alterações de caráter proliferativo ocorrerão quanto menor for o número e a virulência das bactérias e maior a resistência orgânica. A má nutrição (dietas de emagrecimento inadequadas), o estresse e o consumo excessivo de álcool ou drogas podem reduzir a resistência orgânica.
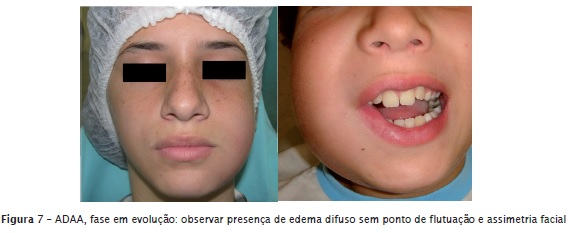
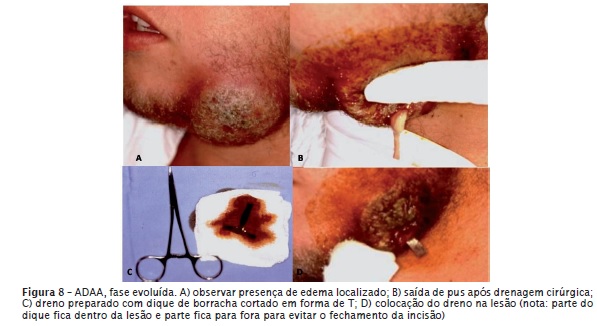
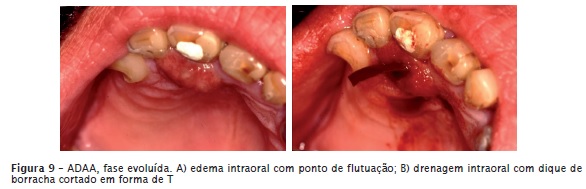
Com o canal contaminado por bactérias e com a presença de pericement ite apica l aguda, as células inflamatórias (principalmente neutrófilos polimorfonucleares) deslocam-se até a região periapical na tentativa de eliminar essas bactérias. Se tal objetivo não é alcançado, ou seja, se as células de defesa não conseguem combater a contaminação bacteriana do canal radicular, há exacerbação do quadro e o processo inf lamatório torna-se agudo purulento ou exsudativo, denominado de abscesso dentoalveolar agudo (ADAA). Esse quadro clínico demanda tratamento de urgência por conta da presença de dor intensa. De acordo com a localização da coleção purulenta, o ADAA classi f ica-se clinicamente em: inicial, em evolução e evoluído. Na fase inicial o pus encontra-se próximo ao forame apical (sem edema); na evoluída invade o trabeculado ósseo e está próximo ao periósteo (edema difuso sem ponto de flutuação – figure 7); na fase em evolução o pus perfura o periósteo e cai em tecido mole (edema localizado com ponto de flutuação). O ponto de flutuação caracterizase por um ponto amarelado sobre o edema significando proximidade do pus com a mucosa (edema intraoral) ou com a pele (edema extraoral). No caso de ADAA na fase evoluída, deve-se fazer drenagem cirúrgica com lâmina de bisturi sobre o ponto de f lutuação para a saída do pus e, a seguir, colocar um dreno para manter aberta a via de drenagem (figuras 8 e 9). Um ADAA não tratado pode evoluir para complicações sistêmicas como osteomielite, angina de Ludwig, dentes de Turner e algumas vezes para óbito.
O tratamento sistêmico para o ADAA consiste em antibioticoterapia e uso de analgésicos/antiinflamatórios e está organizado no quadro III.

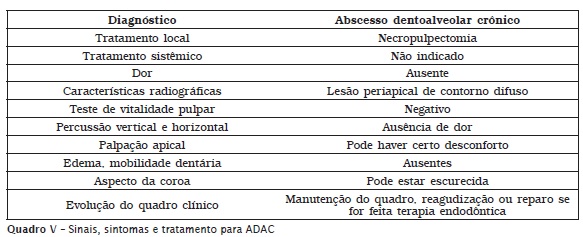
As características clínicas e o tratamento do ADAA estão dispostos no quadro IV. Vale lembrar que todos os tratamentos locais devem ser feitos sob isolamento absoluto.
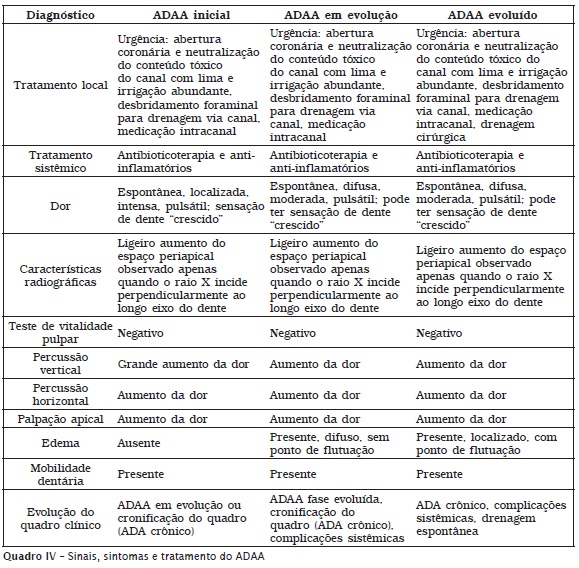
Além dos sinais e sintomas relatados no quadro, o paciente ainda pode apresentar trismo, cefaleia, febre e prostração (abatimento físico).
Após a regressão dos sinais e sintomas clínicos do ADAA, o paciente precisa retornar ao consultório para realização do preparo biomecânico completo do canal radicular e posterior obturação.
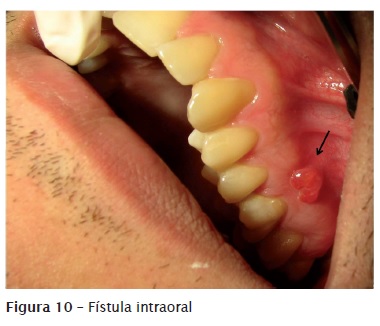
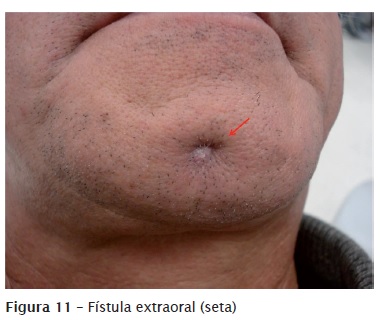
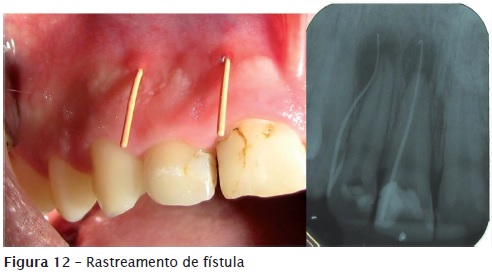
Quando não é feito o tratamento do ADAA, o quadro pode evoluir para a cronificação de um processo agudo. Quando isso acontece, o pus, presente na fase aguda do abscesso, procura saída (drenagem) formando um trajeto por regiões de menor resistência até encontrar a mucosa ou pele; ao encontrar a saída, está instalada a fístula por meio da qual o remanescente purulento é drenado espontaneamente. Assim, em muitos casos de ADAC há a presença de fístula, que pode ser intraoral (figure 10) ou extraoral (figure 11). A fístula não deve jamais ser drenada, pois ela já é a própria drenagem espontânea de remanescente de pus. Para auxiliar na descoberta do dente foco de infecção, ou seja, o dente com ADAC, é possível efetuar o rastreamento da fístula introduzindo nela um contraste como, por exemplo, um cone de guta-percha previamente desinfetado, até encontrar resistência, e então é feita uma radiografia (figure 12). A figure 13 mostra uma imagem de tomografia com a presença do trajeto fistuloso.
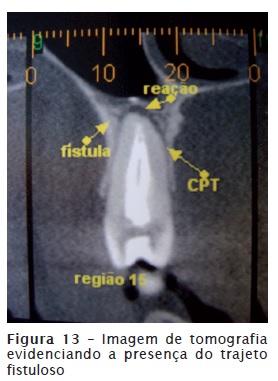
O termo abscesso é empregado em decorrência da presença de coleção purulenta localizada. As palavras agudo e crônico, quando colocadas junto ao termo abscesso, referem-se somente às características e à evolução clínica dessa patologia periapical, pois na maioria das vezes o abscesso apresenta um predomínio de polimorfonucleares, típico de inflamação aguda. O termo agudo indica que o quadro clínico é de rápida evolução; o termo crônico sugere uma evolução mais lenta do processo inflamatório.
Quando a patologia periapical crônica, como granuloma periapical e cisto periapical de origem inflamatória, se instala logo após a pericementite apical aguda, a resposta imunológica diante da presença do agente agressor no canal radicular acarreta o desenvolvimento de uma "lesão" periapical. No entanto o que acontece na região é uma resposta imunológica ou de proteção contra os microrganismos presentes na polpa necrosada e em todo o sistema de canais radicular. Como consequência da infecção pulpar, ocorre a reabsorção do osso esponjoso periapical. Portanto, um exame radiográfico, por gerar imagem bidimensional, não é capaz de mostrar a lesão inicial presente. Já a tomografia computadorizada permite observar a instalação inicial da lesão. Para que a lesão periapical seja vista radiograficamente, é preciso que a cortical óssea vestibular ou lingual/palatina tenha sido reabsorvida pelo processo inflamatório, e para isso ocorrer leva-se meses. Portanto, diante de uma lesão periapical visível radiograficamente sabe-se que a reação inflamatória está ali presente há meses, caracterizando um processo de longa duração. Por ser um processo de longa duração, houve tempo para que ocorresse a proliferação bacteriana por todo o sistema de canais radiculares (túbulos dentinários, canais laterais, canais acessórios, secundários, colaterais, delta apical, canal recorrente – figure 14). Nos processos de longa duração, a contaminação bacteriana não está limitada apenas à luz do canal principal. Diante de tal constatação, recomenda-se colocar medicação intracanal ou curativo de demora entre sessões (à base de hidróxido de cálcio) após o preparo biomecânico de dentes com necrose pulpar e lesão periapical visível radiograficamente. O objetivo dessa medicação é combater os microrganismos que escaparam à ação dos instrumentos endodônticos e das soluções irrigadoras e que conseguem atuar, sobretudo, no canal principal. A figure 15 ilustra a presença de lesão periapical crônica de origem endodôntica.
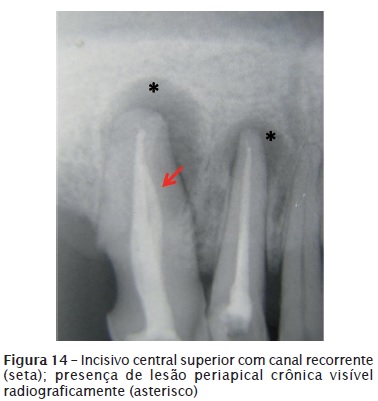
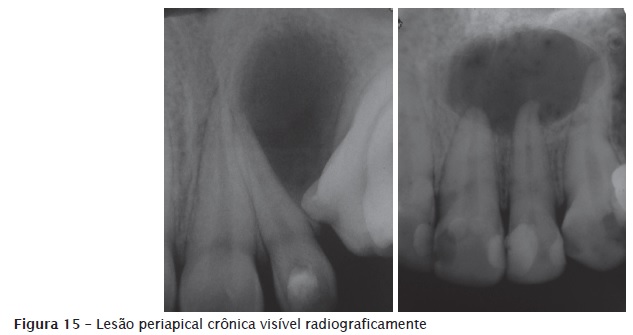
Clinicamente , o paciente não relata sintomatologia dolorosa quando está presente um granuloma periapical ou um cisto periapical de origem inflamatória, a não ser que haja uma mudança na microbiota local (como extravasamento de conteúdo tóxico do canal radicular para a região periapical, durante o tratamento endodôntico) ou uma queda de resistência orgânica, transformando o quadro, que antes era crônico, em agudo, ou seja, ocorrendo a reagudização ou reagudecimento de um processo crônico.
É importante ressaltar que o ADAC também pode sofrer reagudização, pelos mesmos motivos anteriormente descritos, sendo denominado de abscesso dentoalveolar crônico reagudizado. De uma forma geral, quando ocorre reagudização de uma lesão periapical crônica, o quadro é chamado de abscesso fênix (recebe esse nome em analogia à ave que renasce das cinzas). Classifica-se o abscesso fênix de acordo com a localização da coleção purulenta, da mesma maneira que o ADAA: inicial, em evolução e evoluído. O diagnóstico diferencial entre o ADAA e o abscesso fênix é dado pela presença de lesão periapical no abscesso fênix.
Destaque-se que, para o tratamento sistêmico das reagudizações de lesões periapicais crônicas (ADAC, granuloma periapical e cisto de origem inflamatória), há uma diferença na antibioticoterapia, em virtude da presença de microbiota aeróbia grampositiva (da fase aguda) e microbiota anaeróbia gram-negativa (da fase crônica). Nessas situações, prescreve-se uma associação de amoxicilina 500 mg e ácido clavulâmico, de 8 em 8 horas, durante 7 dias. Para o controle da dor, a medicação pode ser a mesma indicada para o ADAA. O tratamento local (endodôntico de urgência) também é o mesmo seguido para todas as fases do ADAA.
Então, a lesão periapical visível radiograficamente (figure 16) deve ser considerada como uma resposta imune periapical, pois é a defesa orgânica do paciente atuando com objetivo de isolar a infecção endodôntica, mantendo-a confinada ao sistema de canais radicular e prevenindo a sua disseminação sistêmica. O infiltrado inf lamatório presente nas lesões periapicais crônicas é um misto de linfócitos T e B, PMNs, macrófagos, plasmócitos, eosinófilos e mastócitos. A diferenciação radiográfica entre granuloma periapical e cisto periapical de origem inflamatória é apenas sugestiva, já que a confirmação só pode ser dada com exames histopatológicos. Entretanto isso não interfere no tratamento local de tais lesões, uma vez que para ambas se indica necropulpectomia.
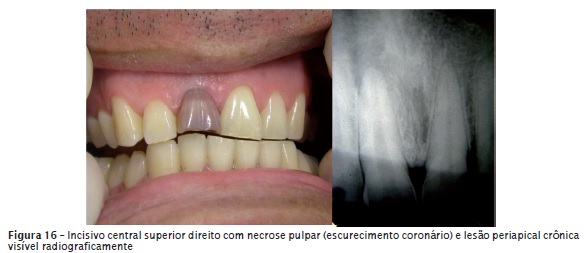
O granuloma periapical é caracterizado pela presença de linfócitos, plasmócitos e macrófagos, os quais estão circundados por uma cápsula fibrosa. No seu interior, pode ou não existir a presença de restos epiteliais. Clinicamente, o granuloma periapical apresenta-se assintomático.
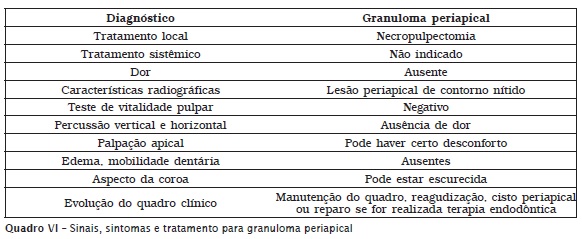
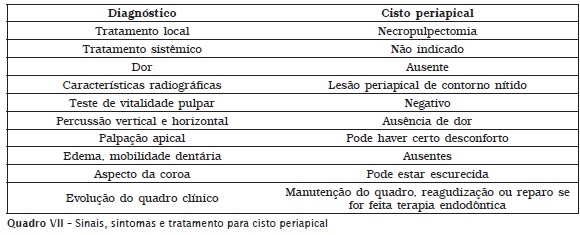
O cisto periapical de origem inf lamatória desenvolve-se a partir do estímulo e da proliferação dos restos epiteliais de Malassez, que são restos da bainha de Hertwig, responsável pelo desenvolvimento radicular. Com o estímulo dos restos epiteliais, dá-se início ao desenvolvimento de uma cavidade cística revestida por epitélio e preenchida por substância líquida ou pastosa. O desenvolvimento e o crescimento do cisto periapical são lentos e podem atingir maiores dimensões e provocar expansão da cortical óssea, dando origem a um edema ou tumefação consistente e indolor. Quando palpada, a tumefação pode causar dor. Clinicamente, o cisto periapical é assintomático e é descoberto durante exames radiográficos de rotina. Os quadros V, VI e VII apresentam as características clínicas e radiográficas das lesões periapicais ADAC, granuloma periapical e cisto periapical de origem inflamatória, respectivamente.
Referências
1. Cardoso RJA, Gonçalves EAN. Endodontia – trauma. São Paulo: Artes Médicas; 2002.
2. Cohen S, Burns R. Procedimentos para o diagnóstico. In: Caminhos da polpa. 6. ed. Rio de Janeiro: Guanabara Koogan; 1997. p. 3-25.
3. Cohen S, Hargreaves KM. Diagnóstico. In: Caminhos da polpa. 9. ed. Rio de Janeiro: Elsevier; 2007. p. 2-39.
4. Estrela C. Dor odontogênica. São Paulo: Artes Médicas; 2001.
5. Estrela C, Figueiredo JA. Métodos de diagnóstico aplicados à endodontia. In: Endodontia – princípios biológicos e mecânicos. São Paulo: Artes Médicas; 1999. p. 25-49.
6. Hargreaves KM, Goodis HE. Polpa dentária – de Seltzer e Bender. São Paulo: Quintessence; 2009.
7. Leonardo MR, Esberard RM, Bonetti Filho I, Leonardo RT, Tanomaru Filho M. Tratamento de canais radiculares: atualidades técnicas. São Paulo: Premier; 1996.
8. Leonardo MR, Leal JM. Endodontia: tratamento de canais radiculares. 3. ed. São Paulo: Panamericana; 1998.
9. Leonardo MR. Semiologia e diagnóstico clínico/ radiográfico das alterações patológicas pulpares. In: Endodontia – tratamento de canais radiculares. Princípios técnicos e biológicos. v. 1. São Paulo: Artes Médicas; 2005. p 21-48.
10. Okeson J. Dores de origem dental. In: Dor orofacial. Guia de avaliação, diagnóstico e tratamento. São Paulo: Quintessense; 1998. p. 130-9.
11. Sayão S et al. Endodontia, ciência, tecnologia e arte. São Paulo: Santos; 2007.
12. Siqueira Jr JF. Tratamento das infecções endodônticas. Rio de Janeiro: Medsi; 1997.
 Endereço para correspondência:
Endereço para correspondência:
Denise Piotto Leonardi
Rua Professor Pedro Viriato Parigot de Souza, n.º 5.300 – Campo Comprido
CEP 81280-330 – Curitiba – PR – Brasil
E-mail: deleonardi@yahoo.com.br