Services on Demand
Article
Related links
Share
Revista da Associacao Paulista de Cirurgioes Dentistas
Print version ISSN 0004-5276
Rev. Assoc. Paul. Cir. Dent. vol.68 n.2 Sao Paulo Apr./Jun. 2014
Efeito de pasta com nanopartículas de hidroxiapatita e fluoreto sobre a desmineralização da dentina
The effect of paste containing hydroxyapatite nanoparticles and fluoride on dentin demineralization
Valéria Di Giacomo I; Lívia Picchi Comar II; Priscila Maria Aranda Salomão III; Ana Carolina Magalhães IV
I Cirurgiã-Dentista pela Faculdade de Odontologia de Bauru da Universidade de São Paulo (FOB/USP)
II Mestre em Ciências Odontológicas pela FOB/USP e aluna de doutorado em Ciências Odontológicas da FOB/USP
III Mestre em Ciências Odontológicas pela FOB/USP e aluna de doutorado em Ciências Odontológicas pela FOB/USP
IV Livre docente pela USP e professora doutora associada da FOB/USP
RESUMO
Este estudo avaliou o potencial de uma formulação experimental à base de HAP e fluoreto de sódio, para reduzir a desmineralização da dentina bovina in vitro. Oitenta e quatro amostras de dentina radicular bovina foram divididas em 7 grupos de 12 amostras, sendo submetidas a um dos seguintes tratamentos: 1) pasta Nanop plus (HAP a 20% + 9.000 ppm F, NaF); 2) pasta Nanop (HAP 20%); 3) pasta F (9.000 ppm F, NaF); 4) pasta placebo (sem HAP e F); 5) MI Paste (caseína e fosfato de cálcio); 6) MI Paste plus (caseína e fosfato de cálcio, 900 ppm F, NaF); 7) sem tratamento (controle). Os tratamentos foram realizados duas vezes ao dia, intercalados por ciclagem de pH (des-remineralização), por 7 dias. Na sequência, as amostras foram analisadas por microdureza superficial e longitudinal (10-220 μm). Os dados foram tabulados e submetidos à análise estatística (p<0,05). Em geral, os únicos tratamentos que tiveram efeito significativo na redução da desmineralização da dentina foram as pastas Nanop plus e F. Portanto, os dados confirmaram que o fluoreto ainda continua sendo o melhor agente químico para controlar a desmineralização dentária. Já a pasta experimental contendo nanopartículas de HAP foi ineficaz em reduzir a desmineralização da dentina utilizando-se o modelo experimental proposto.
Palavras-chave: dentina; desmineralização; fluoretos
ABSTRACT
This study evaluated the potential of an experimental formulation containing HAP and sodium fluoride to reduce bovine dentin demineralization in vitro. Eighty-four bovine roots dentin samples were divided into 7 groups of 12 samples and subjected to one of the following treatments: 1) Nanop plus paste (HAP 20% + 9000 ppm F, NaF); 2) Nanop paste (HAP 20%) 3) F paste (9000 ppm F, NaF); 4) placebo paste (without HAP and F); 5) MI paste (casein and calcium phosphate); 6) MI Paste plus (casein and calcium phosphate, 900 ppm F, NaF); 7) no treatment (control). The treatments were performed twice a day, interspersed by pH cycling (de-remineralization) for 7 days. Thereafter, the samples were analyzed using surface and cross-sectional microhardness (10-220 μm). The data was plotted and statistically analyzed (p<0.05). The treatments that produced a significant effect on the reduction of dentin demineralization were Nanop plus and F pastes only. Therefore, the data confirmed that fluoride is still the best chemical agent to control dental demineralization. The experimental paste containing HAP nanoparticles was ineffective in reducing dentin demineralization when using this experimental model.
Keywords: dentin; demineralization; fluoride
RELEVÂNCIA CLÍNICA
As pastas com nanopartículas de HAP poderiam ser uma alternativa para reduzir lesões cariosas iniciais em dentina, porém o experimento mostrou que pastas contendo 9.000 ppm F continuam sendo as melhores opções para estes casos.
INTRODUÇÃO
A cárie dentária é uma lesão relacionada à desmineralização dos tecidos dentários promovida pela exposição aos ácidos de origem microbiana, que se estabelece em pacientes que apresentam biofilme dentário cariogênico e dieta rica em açúcar.1 O principal ácido liberado pelos microrganismos é ácido lático, que induz à redução do pH ao redor de 5,0 em um biofilme com uma matriz rica em minerais, gerando uma desmineralização inicial de subsuperfície, caracterizada clinicamente como mancha branca (primeiro sinal clínico da lesão). Durante este estágio, ainda é possível reverter o processo por procedimentos minimamente invasivos, evitando-se a cavitação e consequentemente reabilitação mais complexa, cara e dolorosa.
No contexto da Cariologia, a aplicação ou reposição de cálcio e fosfato perdidos das superfícies desmineralizadas e a formação de uma película/camada protetora de hidroxiapatita (HAP) poderia refletir em resultados promissores na redução da desmineralização e no aumento da remineralização da estrutura dentária.2
Neste sentido, foi lançado um produto australiano chamado Prospec MI Paste (GC América Inc., contendo RECALDENT-CPP-ACP), à base de fosfato de cálcio e fosfopeptídeo da caseína, uma molécula naturalmente presente no leite, que é capaz de ligar íons cálcio e fosfato, estabilizando-os na forma de fosfato de cálcio amorfo. Este produto apresenta propriedades remineralizantes assim como propriedades preventivas contra o aparecimento de novas lesões cariosas ou a progressão de lesões cariosas pré-existentes, com promissores resultados laboratoriais e clínicos. O fosfato de cálcio amorfo, em condições apropriadas, trabalha com precursor da hidroxiapatita (HAP) promovendo a remineralização da estrutura dentária.3-8
No Brasil foi desenvolvido um produto à base de nanopartículas de HAP, com o objetivo de promover a remineralização e o tratamento da hiperestesia dentinária. As nanopartículas apresentam elevada área superficial, o que pode facilitar a disponibilidade do produto e a reorganização dos íons cálcio e fosfato na forma de HAP sobre o tecido desmineralizado.9-11 No entanto, a reatividade da HAP nanopartículada depende do tamanho e formato da partícula. Considera-se nanopartícula, quando o tamanho da partícula é menor que 100 nm.
Destaca-se que atualmente a clínica odontológica é desprovida de materiais remineralizantes e dessensibilizantes baseados em nanotecnologia. Várias pesquisas testando produtos similares contendo nano-hidroxiapatita, realizadas em outros países, têm mostrado resultados positivos na remineralização de lesões artificiais de cárie em esmalte utilizando ciclagem de pH,12-14 assim como em dentina15, apesar das formulações não serem capazes de remineralizar o dente totalmente. Além do fato de haver poucos estudos sobre este tópico, a maioria dos trabalhos dá enfoque ao esmalte e não temos informação sobre o potencial desta nova formulação com nano-HAP na prevenção da desmineralização da dentina.
Portanto, este trabalho teve como objetivo avaliar o potencial de uma formulação experimental à base de nanopartículas de HAP e fluoreto de sódio, em reduzir a desmineralização da dentina bovina in vitro, utilizando como variáveis de resposta a microdureza superficial e longitudinal.
MATERIAIS E MÉTODOS
Preparação das amostras e grupos experimentais
Para o estudo foram utilizadas amostras de dentina (4 mm x 4 mm), obtidas de fatias da região cervical da raiz, através de uma secção no sentido vestíbulo-lingual realizada utilizando uma máquina de corte de precisão ISOMET Low Speed Saw (Buehler Ltd, Lake Bluff, IL, EUA) e dois discos diamantados de dupla face - XL 12205, "High concentration", 102 x 0,3 x 12,7 mm3 (Extec Corp., Enfield, CT, EUA) e um espaçador de 4 mm de espessura. A partir desta fatia, duas amostras de dentina foram obtidas através de uma secção dupla no sentido vestíbulo-lingual e uma única no sentido mésio-distal. Em seguida, as amostras de dentina foram inseridas no centro de discos de acrílico com Cerafix para possibilitar a planificação. Para isso, utilizaram-se uma politriz (Arotec, Cotia, SP, Brasil) e lixas de carbeto de silício de granulação 320, 600 e 1200 (Extec Corp., Enfield, CT, EUA). Entre as trocas de lixas e ao final do polimento, as amostras foram lavadas em ultrassom T7 Thornton (Unique Ind. e Com. de produtos Eletrônicos Ltda., Indaiatuba, SP, Brasil), durante cinco minutos, com água deionizada.
Posteriormente, as amostras passaram pela avaliação da microdureza superficial (diamante KNOOP-KHN, 10 g, 15 s, Buehler Omnimet, Lake Bluff, IL, EUA) através da realização de cinco endentações a uma distância de 100 μm entre elas no centro da superfície da amostra. As amostras foram aleatoriamente divididas nos grupos experimentais de acordo com os valores de microdureza de superfície iniciais (n=12, total 84 amostras): pastas experimentais 1) Nanop plus (HAP 20% + 9.000 ppm F, NaF, FGM-Dentscare, Joinville, SC, Brasil); 2) Nanop (HAP 20%, FGM-Dentscare, Joinville, SC, Brasil); 3) F (9.000 ppm F, NaF, FGM-Dentscare, Joinville, SC, Brasil); 4) placebo (sem composto ativo, FGM-Dentscare, Joinville, SC, Brasil); 5) MI Paste (caseína e fosfato de cálcio, GC America, Alsip, IL, EUA); 6) MI Paste plus (caseína e fosfato de cálcio, 900 ppm F, NaF, GC America, Alsip, IL, EUA); 7) sem tratamento (controle).
As pastas experimentais produzidas pela FGM/Dentscare tinham como composição básica: nitrato de potássio, água destilada, espessante, surfactante, umectante, adoçante, flavorizante e preservantes.
Ciclagem de pH e tratamento
As amostras de dentina foram protegidas em 2/3 da superfície (controle) utilizando-se esmalte cosmético de unha vermelho, deixando o centro da superfície exposto.
Posteriormente, as amostras foram submetidas à ciclagem de pH, sendo imersas em solução desmineralizante (Ca a 1,5 mM, P a 0,9 mM, ácido acético a 50 mM, pH 5,0, 37º C, v=30 mL/bloco) por 8h e em solução remineralizante (HEPES tampão a 20 mM, Ca a 1,5 mM, P a 0,9 mM, KCl a 130 mM, NaN3 a 5 mM, pH 7,0, 37º C, v=30 mL/bloco) por 16h, sem agitação durante 7 dias, a 37oC.16,17
Durante os 7 dias de ciclagem, as pastas experimentais foram aplicadas em uma quantidade pré-determinada utilizando um microaplicador, durante 1 minuto de forma passiva, 2x/dia, antes e após a exposição à solução desmineralizante. O excesso de pasta foi removido com cotonete de forma que nenhuma pasta estivesse visível sobre as amostras e, em seguida, as amostras foram novamente imersas em uma das soluções.
Análise da microdureza superficial e longitudinal
A microdureza superficial final foi avaliada conforme descrito anteriormente para o cálculo da porcentagem de perda de microdureza de superfície (%PDS).
Na sequência, as amostras foram seccionadas longitudinalmente, embutidas em resina acrílica e polidas para a análise da microdureza longitudinal em uma sequência de 3 endentações a distâncias de 10, 30, 50, 70, 90, 110 e 220 μm da superfície, utilizando o mesmo peso e tempo já descritos. As médias de microdureza para cada distância foram calculadas (KHN).
Análise estatística
Os dados foram tabulados em planilhas de Excel para o cálculo da média e desvio-padrão e analisados utilizando programa GraphPad Prism 4 (Graph Pad Software, EUA). As médias de microdureza superficial e longitudinal foram comparadas utilizando-se ANOVA a dois critérios, seguida pelo teste de Bonferroni, considerando como variáveis os grupos experimentais e as profundidades. O nível de significância adotado foi de 5%.
RESULTADOS
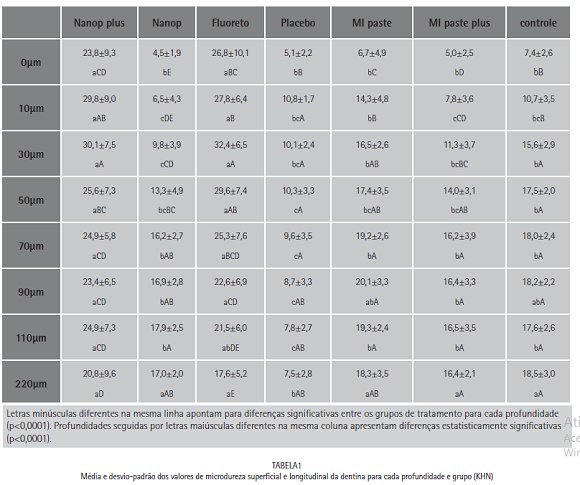
Pode-se notar que as pastas mais eficazes em reduzir a desmineralização superficial, considerando que a microdureza da dentina sadia varia entre 20-70 KHN, foram aquelas contendo fluoreto (Nanop plus e F). Em relação à microdureza superficial, as médias de %PDS (desmineralização superficial) encontradas foram: 1) pasta Nanop plus (34,4±29,8); 2) pasta Nanop (86,3±9,6); 3) pasta F (35,9±39,9); 4) pasta placebo (85,9±7,0); 5) MI Paste (81,9±11,9); 6) MI Paste plus (85,3±9,3); 7) sem tratamento (79,6±9,8).
Em relação à microdureza longitudinal (desmineralização em profundidade), o mesmo resultado na comparação entre os tratamentos foi obtido até 70 μm de profundidade. As outras pastas apresentaram um comportamento similar à pasta placebo
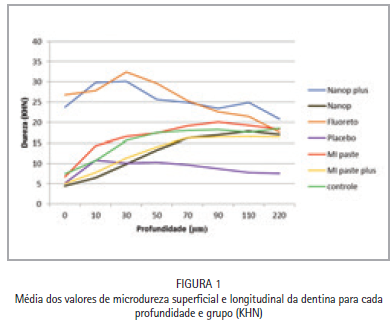
e controle, sendo que as amostras tratadas com a pasta placebo apresentaram microdureza significativamente menor que as do controle a partir de 50 μm de profundidade (Tabela 1 e Figura 1).
Os valores de microdureza da dentina ainda se apresentaram baixos aos 220 μm de profundidade para todos os grupos, com exceção daqueles contendo fluoreto (Nanop plus e F). O efeito preventivo das duas pastas contendo fluoreto contra a desmineralização foi similar e mais pronunciado nas camadas mais superficiais da dentina.
DISCUSSÃO
De acordo com os resultados, somente as pastas experimentais contendo fluoreto foram efetivas na redução da desmineralização da dentina. Estes resultados foram diferentes de um estudo prévio em que uma pasta similar contendo Nanop a 20%, porém com apenas 900 ppm F (ao invés de 9.000 ppm F como no presente estudo), foi incapaz de reduzir a desmineralização do esmalte e dentina in vitro.9 No estudo anterior, somente a pasta com 900 ppm F (sem HAP) reduziu a desmineralização do esmalte e dentina. 9 Dessa forma, podemos inferir que a adição de uma maior concentração de fluoreto à pasta com Nanop no presente trabalho (10x maior que no trabalho anterior) foi responsável pelo efeito positivo, minimizando possíveis interações entre fluoreto e HAP dentro da pasta e a consequente redução da biodisponibilidade de fluoreto. Portanto, o efeito preventivo da Nanop plus parece não estar relacionado à presença das nanopartículas de HAP, mas sim ao efeito do fluoreto em reduzir a desmineralização.
Os dados confirmaram que o fluoreto ainda continua sendo o melhor agente químico para controlar a desmineralização dentária. A presença de fluoreto nos fluídos bucais (em especial o fluído do biofilme) durante o desafio ácido favorece a sua adsorção à HAP, inibindo a desmineralização. Quando o pH é restabelecido, traços de fluoreto no ambiente pode torná-lo supersaturado em relação à FAP (fluorapatita), acelerando o processo de remineralização.18
No presente estudo, a pasta contendo apenas HAP (Nanop) foi ineficaz em reduzir a desmineralização dentária. Para um melhor entendimento do efeito das pastas experimentais sobre a estrutura dentária, a quantidade de cálcio e fosfato liberada das pastas em água foi avaliada. As pastas experimentais apresentaram concentrações de cálcio e fosfato solúveis muito reduzidas, inclusive semelhantes ao placebo, isto é, a solubilidade da HAP adicionada às pastas Nanop foi muito baixa e, desta forma, quantidades irrelevantes de cálcio e fosfato poderiam estar disponíveis para interagir com a superfície dentária.9 Por outro lado, poderia imaginar que apesar da baixa solubilidade da HAP, as nanopartículas poderiam interagir com o tecido dentário dentro dos poros da lesão cariosa por embricamento mecânico, devido ao pequeno tamanho das partículas. No entanto, este efeito não deve ter ocorrido no presente modelo experimental, uma vez que a pasta com Nano-HAP apenas não teve efeito contra a desmineralização da dentina. Seria interessante testar futuramente se o tempo e a forma de aplicação (passiva ou ativa) poderiam ter influência sobre o efeito da pasta no tecido dentário ou se o uso de pastas contendo partículas ainda menores de HAP poderia apresentar maior reatividade. Ainda seria interessante avaliar se a concentração de HAP teria alguma influência no resultado. No presente estudo nós testamos a concentração de 20% de HAP, no entanto, estudos anteriores testaram concentrações de HAP variando de 1 a 20%.9,12-15
Outra forma de melhorar a eficácia das pastas experimentais seria a associação de nanopartículas de sílica com nanopartículas de HAP, uma vez que estudo prévio mostrou que o colágeno quando infiltrado por partículas de sílica serve de arcabouço para as nanopartículas de HAP, tornando o ambiente favorável à remineralização.10
Uma vez que estudos prévios têm mostrado efeito positivo da Nano-HAP sobre a remineralização dentária12-15 é provável que diferentes modelos de ciclagem de pH focando na remineralização de lesões pré-formadas também poderiam apontar resultados mais favoráveis para o uso da pasta experimental que em relação à prevenção da desmineralização usando este modelo de ciclagem de pH.
O uso da pasta experimental contendo nano-HAP e fluoreto também parece promissor para o controle da hiperestesia dentinária como demonstrado em estudo clínico.11 Portanto, também não se pode descartar como mecanismo de ação da pasta experimental contendo nano-HAP e F a possível obliteração dos túbulos dentinários.
É importante ressaltar que os resultados de estudos laboratoriais não devem ser extrapolados diretamente para a situação clínica, uma vez que o ambiente bucal é mais complexo que o modelo de laboratório. Portanto, devemos considerar a hipótese de que in vivo o efeito das pastas experimentais poderia ser mais favorável pela presença da saliva humana e do fluído dentinário como demonstrado em estudo clínico.11 Dessa forma, além dos estudos testando a forma de aplicação e concentração de HAP na pasta assim como o seu efeito na remineralização, as pastas experimentais devem ser futuramente testadas em um modelo in situ para averiguar o comportamento no ambiente bucal.
A inclusão das pastas placebo e com fluoreto no delineamento experimental possibilitou testar e comparar corretamente o efeito de cada agente ativo adicionado. Como controle comercial, as pastas MI paste (com e sem F) foram inclusas no estudo, pois, apesar de terem composição distinta das pastas experimentais, apresentam mecanismo de ação e aplicação similares às pastas Nanop. Produtos contendo CPP-ACP têm habilidade de prevenir a desmineralização e aumentar a remineralização de dentina pela biodisponibilidade do cálcio e fosfato in vitro,19-21 porém dados opostos têm sido demonstrados no estudo de Pulido et al.22 e no presente trabalho. Apesar das pastas contendo CPP-ACP apresentarem uma quantidade de cálcio e fosfato solúvel maior que as pastas experimentais Nanop9, estas não foram capazes de reduzir significativamente a desmineralização da dentina, utilizando este protocolo experimental de ciclagem de pH.9
As pastas contendo CPP-ACP ainda têm mostrado aumentar a remineralização de lesões naturais in vivo.4,7 No entanto, devido à falta de estudos clínicos controlados, randomizados e longitudinais, ainda não há evidência científica convincente sobre o efeito cariostático do CPP-ACP.23 Recentemente, um estudo clínico randomizado, controlado e longitudinal mostrou que a aplicação diária de CPP-ACP a 10% não teve efeito aditivo em relação ao uso do dentifrício fluoretado no controle da cárie em pré-escolares por um período de 1 ano.24 Infelizmente não há estudos clínicos realizados em adultos para tratamento de cárie radicular.
Portanto, futuros estudos in situ devem ser realizados para averiguar o efeito cariostático das pastas Nanop com ou sem fluoreto sobre a desmineralização e remineralização dentária. Somente com estes resultados, estudos clínicos poderão ser delineados.
CONCLUSÃO
A pasta experimental contendo nanopartículas de HAP foi ineficaz em reduzir a desmineralização da dentina. As únicas pastas eficazes em reduzir a desmineralização foram aquelas contendo 9.000 ppm de fluoreto. Portanto, as pastas fluoretadas (Nanop plus e F), como método caseiro adicional ao uso de dentifrício fluoretado, poderiam ser uma estratégia interessante para pacientes adultos com risco ao desenvolvimento de lesão de cárie radicular.
APLICAÇÃO CLÍNICA
As pastas contendo fluoreto podem ser indicadas para pacientes adultos como método adicional à escovação diária em casos de lesões iniciais de cárie radicular, evitando procedimentos mais invasivos, como restaurações.
AGRADECIMENTO
Ao Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq), Processo: 2514/2011 PIBIC, pelo apoio financeiro concedido durante a realização deste trabalho de Iniciação Científica.
REFERÊNCIAS
1. ten Cate JM, Larsen MJ, Pearce EIF, Fejerskov O. Interações químicas entre dentes e fluídos bucais. In: Fejerskov O, Kidd E. Cárie Dentária. A doença e seu tratamento. 2005:49-70. [ Links ]
2. Cochrane NJ, Cai F, Huq NL, Burrow MF, Reynolds EC. New approaches to enhanced remineralization of tooth enamel. J Dent Res 2010;89:1187-97.
3. Oshiro M, Yamaguchi K, Takamizawa T, Inage H, Watanabe T, Irokawa A, et al. Effect of CCP-ACP paste on tooth mineralization: an FE-SEM study. J Oral Sci 2007;49:115-20.
4. Morgan MV, Adams GG, Bailey DL, Tsao CE, Fischman SL, Reynolds EC. The anticariogenic effect of sugar-free gum containing CPP-ACP nanocomplexes on approximal caries determined using digital bitewing radiography. Caries Res 2008;42:171-84.
5. Yengopal V, Mickenautsch S. Caries preventive effect of casein phosphopeptide-amorphous calcium phosphate (CPP-ACP): a meta-analysis. Acta Odontol Scand 2009;67:321-32.
6. Paggio C, Lombardini M, Dagna A, Chiesa M, Bianchi S. Protective effect on enamel demineralization of a CPP–ACP paste: an AFM in vitro study. J Dent 2009;37:949-54
7. Bailey DL, Adams GG, Tsao CE, Hyslop A, Escobar K, Manton DJ, et al. Regression of post-orthodontic lesions by a remineralizing cream. J Dent Res 2009;88:1148-53.
8. Zhang Q, Zou J, Yang R, Zhou X. Remineralization effects of casein phosphopeptide-amorphous calcium phosphate crème on artificial early enamel lesions of primary teeth. Int J Paediatr Dent 2011;21(5):374-81.
9. Comar LP, Souza BM, Gracindo LF, Buzalaf MAR, Magalhães AC. Impact of experimental Nano-HAP Pastes on Bovine Enamel and Dentin Submitted to a pH Cycling Model. Braz Dent J 2013;24(3):273-8.
10. Besinis A, van Noort R, Martin N. Infiltration of demineralized dentin with silica and hydroxyapatite nanoparticles. Dent Mater 2012;28:1012-23.
11. Wang L, Magalhães AC, Araújo D, Francisconi LF, Calabria MP, Buzalaf MAR, et al. Clinical Performance of new agents on reduction of dentinal hypersensitity. In: 90th General Session and Exhibition of the IADR. J Dent Res 2012;91B:1384
12. Huang SB, Gao SS, Yu HY. Effect of nano-hydroxyapatite concentration on remineralization of initial enamel lesion in vitro. Biomed Mater 2009;4:034104.
13. Huang S, Gao S, Cheng L, Yu H. Combined effects of nano-hydroxyapatite and Galla chinensis on remineralisation of initial enamel lesion in vitro. J Dent 2010;38(10):811-9.
4. Huang S, Gao S, Cheng L, Yu H. Remineralization Potential of Nano-Hydroxyapatite on Initial Enamel Lesions: An in vitro Study. Caries Res 2011;45(5):460-8.
15. Tschoppe P, Zandim DL, Martus P, Kielbassa AM. Enamel and dentine remineralization by nano-hydroxyapatite toothpastes. J Dent 2011;39(6):430-7.
16. Lagerweij MD, ten Cate JM. Acid susceptibility at various depths of pH-cycled enamel and dentin specimens. Caries Res 2006;40:33-7.
17. ten Cate JM, Arends J. Remineralization of artificial enamel lesions in vitro. II. Determination of activation energy and reaction order. Caries Res 1978;12:213-22.
18. Buzalaf MA, Pessan JP, Honório HM, ten Cate JM. Mechanisms of action of fluoride for caries control. Monogr Oral Sci 2011;22:97-114.
19. Yamaguchi K, Miyazaki M, Takamizawa T, Inage H, Kurokawa H. Ultrasonic Determination of the Effect of Casein Phosphopeptide-Amorphous Calcium Phosphate Paste on the Demineralization of Bovine Dentin. Caries Res 2007;41(3):204-7.
20. Rahiotis C, Vougiouklakis G. Effect of a CPP-ACP agent on the demineralization and remineralization of dentin in vitro. J Dent 2007;35(8):695-8.
21. Kumar VL, Itthagarun A, King NM. The effect of casein phosphopeptide-amorphous calcium phosphate on remineralization of artificial caries-like lesions: an in vitro study. Aust Dent J 2008;53(1):34-40.
22. Pulido MT, Wefel JS, Hernandez MM, Denehy GE, Guzman-Armstrong S, Chalmers JM, et al. The inhibitory effect of MI paste, fluoride and a combination of both on the progression of artificial caries-like lesions in enamel. Oper Dent 2008;33(5):550-5.
23. Azarpazhooh A, Limeback H. Clinical efficacy of casein derivatives: a systematic review of the literature. J Am Dent Assoc 2008;139(7):915-24.
24. Sitthisettapong T, Phantumvanit P, Huebner C, Derouen T. Effect of CPP-ACP Paste on Dental Caries in Primary Teeth: A Randomized Trial. J Dent Res 2012;91(9):847-52.
 Endereço para correspondência:
Endereço para correspondência:
Ana Carolina Magalhães
Departamento de Ciências Biológicas - FOB/USP
Al. Octávio Pinheiro Brisolla, 9-75 Bauru - SP
17012-901
e-mail: acm@usp.br
Recebido: jan/2014
Aceito: mar/2014